Introducción
En los últimos años hemos tratado de entender las fases de la respuesta inmune, la patogénesis y la protección conferida por vacunas frente a los desafíos de Salmonella Enteritidis, pero debemos tener en cuenta que esa respuesta inmune depende del serotipo infectante y de la expresión genética del huésped. La Salmonella Enteritidis y la S. Typhimurium pueden infectar diversos hospedadores. En las aves comerciales, la infección del tubo gastrointestinal por Salmonella Enteritidis, particularmente en el ciego, puede persistir por varios meses (1). Por el contrario, la Salmonella entérica serovar Gallinarum y serovar Gallinarum biotipo Pullorum causan una enfermedad sistémica en las aves domésticas (2). La S. Gallinarum es causante de la enfermedad denominada Fiebre Tifoidea Aviar, que se presenta como una infección sistémica grave caracterizada con síntomas patológicos como hepatomegalia, esplenomegalia, anemia y una fuerte hemorragia en el tubo gastrointestinal. En trabajos experimentales, S. Gallinarum causó una mortalidad del 60% en pollos de tres semanas de edad (3). S. Gallinarum ha sido controlada en Norte América y en Europa, pero en Suramérica se presentan brotes constantemente (4,2); Chacón et al., 2017 realizó un estudio de secuenciación en Colombia donde reportó la presencia de la bacteria en ponedoras comerciales y pollos de engorde con una mortalidad del 8% (5).
Una de las características más importantes de la S. Gallinarum es que desarrolla un estado de “Portador Persistente”, esto conduce a una infección del tracto reproductivo que causa deformidades en los óvulos y además se produce transmisión a los huevos y a la progenie, perpetuando la enfermedad (2).

La única manera de reparar un sistema mal diseñado es volver a construirlo, si es posible.
Donella Meadows (2015) Pensar en sistemas, Un manual de iniciación
1. Respuesta biológica a la infección por Salmonella spp.
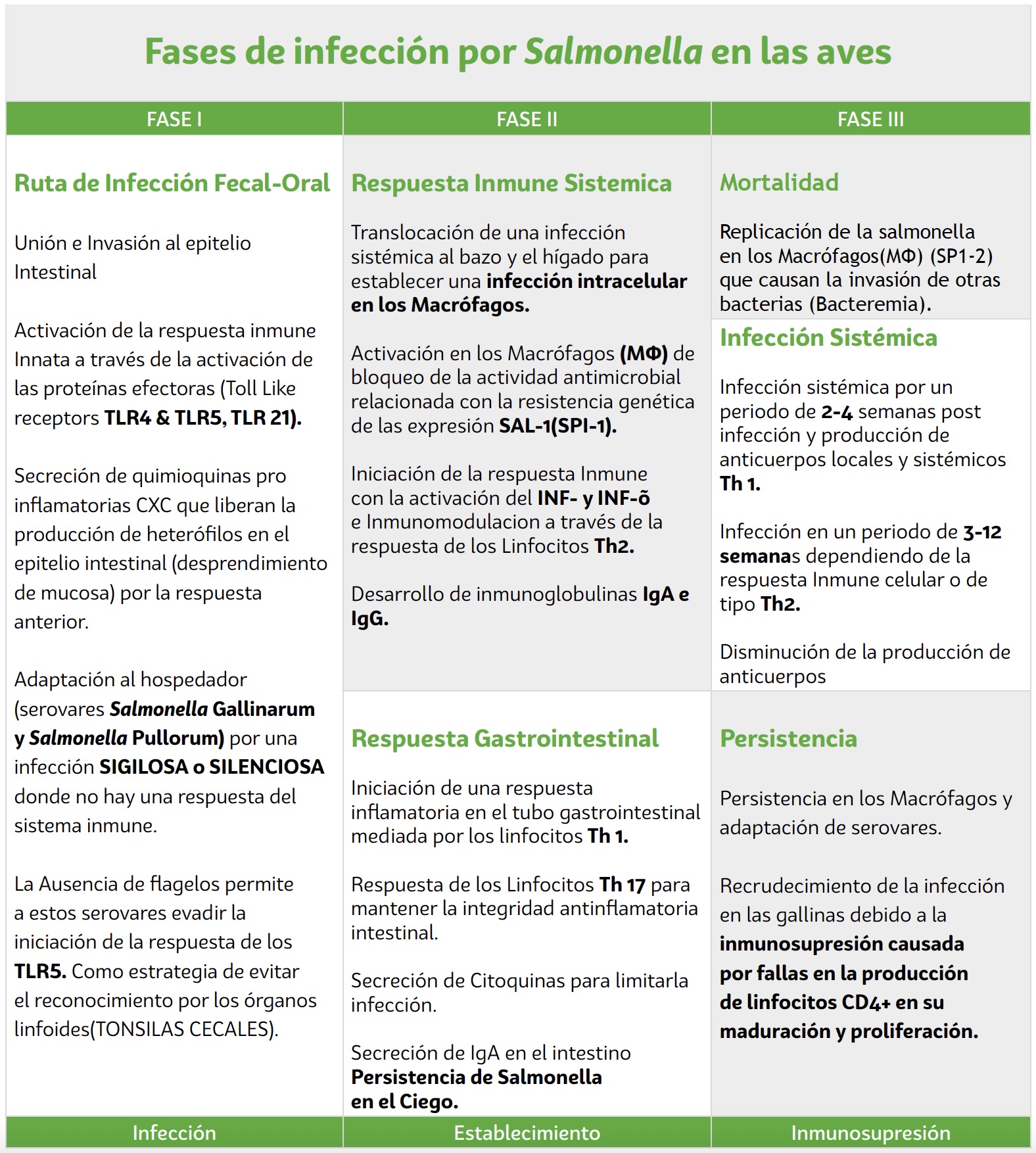
La infección sistémica por Salmonella se presenta en tres fases diferentes de invasión, con una interacción muy significativa con el sistema inmune en cada una. La primera es la fase de invasión del tracto gastrointestinal, la segunda fase es una infección sistémica caracterizada por la invasión intracelular en los macrófagos (MΦ) y finalmente en la tercera fase la eliminación de la bacteria por respuesta del sistema inmune, o donde el ave sucumba a la infección o desarrolle un estado de portador persistente (Tabla 1)(6).
2. Fase 1: Invasión en el tracto gastrointestinal
La SG (Salmonella Gallinarum) luego de ser ingerida, pasa a través del buche que posee un ambiente ácido suave (pH de 4.5) el cual es usado por la bacteria como un mecanismo de adaptación que facilita el paso a través del proventrículo y la molleja (7). Posteriormente, pasa al intestino delgado, especialmente a las células M que interactúan con las placas de Peyer; luego el principal sitio de colonización son los ciegos, ubicados desde la parte distal del íleon hasta el colon. Una de las características más importantes es que la SG es una bacteria autótrofa natural (aquella que requiere la presencia de un nutriente específico en su medio de cultivo para poder crecer y multiplicarse) porque estas bacterias son pobres colonizadoras (7). Por otro lado, las tonsilas cecales cumplen una función inmunomoduladora fuerte ya que son los órganos linfoides secundarios del tracto gastrointestinal de las aves; hay evidencia científica que reporta un agrandamiento en el tejido luego de una infección experimental con SG (8). En las aves, la infección del tracto gastrointestinal por S. Typhimurium produce una respuesta inmune inflamatoria caracterizada por una alta afluencia de heterófilos, mientras que en el desafío por S. Gallinarum y S. Pullorum se produce una inflamación muy limitada (9).
El proceso inflamatorio conduce a la expresión de quimiocinas proinflamatorias CXCLi1 y CXCLi2 y la IL-6, IL-8 (10) al hacer desafíos con S. Typhimurium (11) (Figura 1). En contraste, bajo desafíos de laboratorio con S. Gallinarum estas quimiocinas presentaron una disminución en su expresión (10,12); dicha respuesta inmunológica proinflamatoria se debe al reconocimiento de Salmonella spp. por los receptores tipo Toll como TLR-5 (TLR: Toll like Receptor) el cual reconoce los flagelos de la bacteria que activa la molécula adaptadora MyD88 (Myeloid differentiation primary response gene 88), la cual sirve de conexión entre los TLRs y la vía interna de señalización con el factor de transcripción NF-kB que ingresa al núcleo y activa varios genes de la respuesta inmune innata y consecuentemente la inflamación (13). Winthanage. et al., 2005(10), en desafíos de aves de 1 día de edad con S. Typhimurium, demostró una fuerte respuesta inflamatoria inducida por la expresión de las citoquina y quimiocinas IL-1B, IL-6, CXCLi1 y CXCLi2, teniendo presente que los genes que expresan los flagelos (fli-M) que promueven el estímulo de las islas de patogenicidad 1(SPI-1 TIPO III) fueron fuertemente estimulados. Este sistema capacita a la bacteria para translocarse vía sistémica a los órganos internos que son inmunológicamente expresados por este serotipo de Salmonella. Por su parte, en desafíos con cepas de S. Typhimurium con mutaciones en el gen (fli-M), que expresaron la ausencia de flagelos, la infección redujo fuertemente la expresión de IL-1B, IL-6, CXCLi1 y CXCLi2 (14). Estos hallazgos sugieren que, tanto los flagelos como el sistema SPI-1, están involucrados en la respuesta inmune y la inflamación intestinal. La ausencia de dichos flagelos en Salmonella Gallinarum y S. Pullorum podría ser ventajoso para evadir el reconocimiento por los TLR 5 y que conduce a crear un sistema denominado evasión sigilosa que es el que causa una infección sistémica por SG (14).
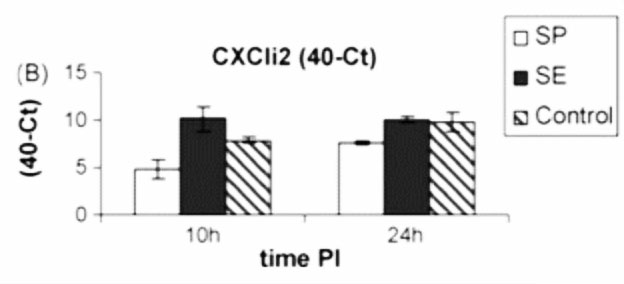
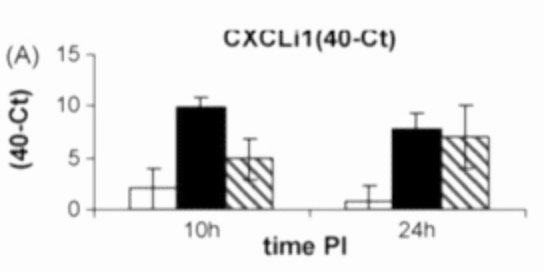
Adaptado de Chapell., et al 2009(11). Expresión de quimiocinas CXC en el íleon de pollitos de un día a 72 horas tras una infección oral con Salmonella. Los niveles relativos de expresión de CXCLi1 (A) y CXCLi2 (B), determinados mediante qRT-PCR, muestran que la infección por S. Enteritidis produce un aumento de la expresión de CXCLi1 (asociada a macrófagos) y CXCLi2 (asociada a heterófilos) en comparación con los controles con infección simulada. Por el contrario, la infección por S. Pullorum induce una disminución de la expresión de quimiocinas. Esto concuerda con la ausencia de infiltración inflamatoria observada tras la infección por S. Pullorum y respalda la teoría de la invasión no inflamatoria por serovares de Salmonella específicos del hospedador aviar. Los datos se expresan como valores de 40-Ct para permitir la comparación de la expresión con aves no infectadas. 40-Ct representa el número máximo de ciclos (40) menos el valor umbral de detección (Ct). Cuanto mayor sea el valor de 40-Ct, mayor será el nivel de expresión génica.
Kaiser, P et al., (2000)(12) reportaron la expresión de la IL-6 y la expresión de las moléculas proinflamatorias en aves desafiadas con SG comparadas con otras salmonelas. Los resultados observados de la actividad de la IL-6 (μg/mL) (tabla 2) fueron S. Typhimurium F98 (77.18 μg/mL), S. Gallinarum (9.02 μg/mL), S. Dublin (77.37 μg/mL), S. Enteritidis (91.14 μg/mL) y E. coli K12(20.82 μg/mL). Por lo tanto, se concluye que la invasión de S. Gallinarum produce poca o ninguna producción de IL-6, lo cual sugiere que la entrada de SG no desencadena una respuesta inmunitaria o inflamatoria fuerte; dicho mecanismo permitiría la entrada sin daño intestinal y podría no desencadenar una respuesta eficaz del huésped, lo que permitiría el desarrollo de una enfermedad sistémica.
3. Fase 2: Infección Sistémica
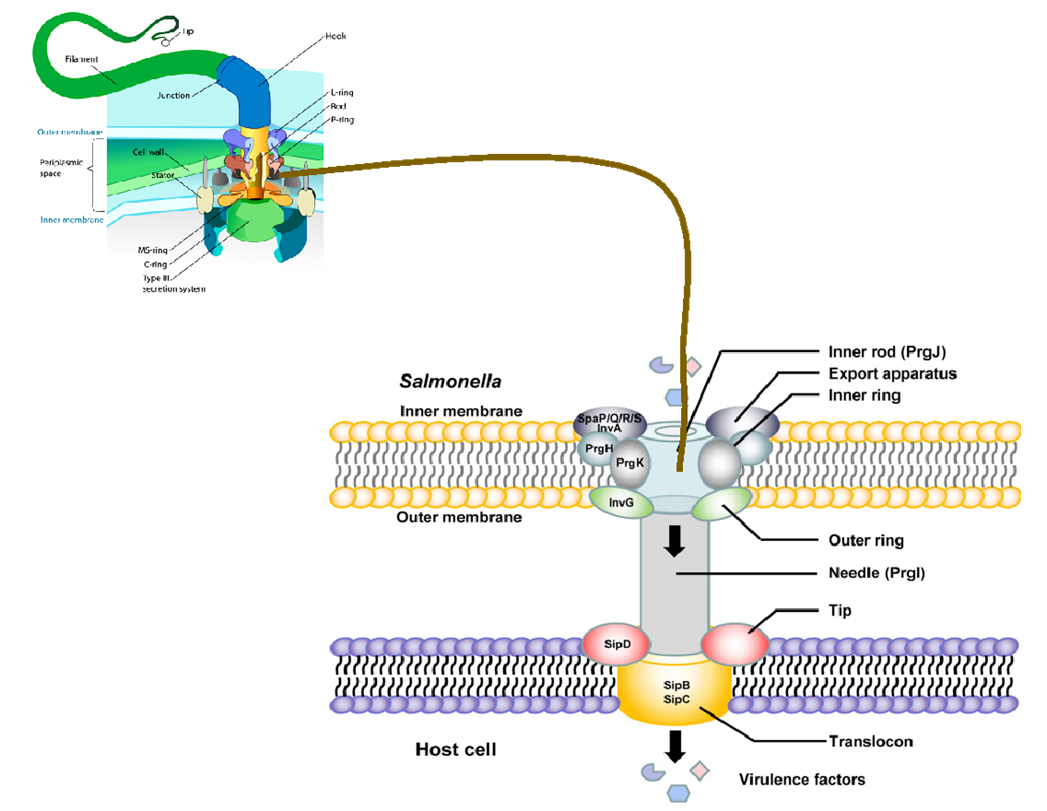
Luego de la invasión en las células gastrointestinales, las especies patógenas de Salmonella invaden las células epiteliales intestinales no fagocíticas mediante el suministro de un conjunto especializado de efectores a través de una maquinaria sofisticada que comprende el sistema de secreción tipo 3 (T3SS), que desempeña un papel crucial en la patogénesis. La bacteria emplea dos T3SS codificados por la isla de patogenicidad 1 de Salmonella (SPI-1) y la isla de patogenicidad 2 de Salmonella (SPI-2). SPI-1 es un grupo génico compuesto por una región de 40 kb que incluye 39 genes que codifican T3SS-1 y sus chaperonas y proteínas efectoras, así como algunos reguladores transcripcionales que controlan la expresión de numerosos genes de virulencia ubicados dentro y fuera de SPI-1 (15). La (SPI-1) desempeña un papel crucial en la interacción entre Salmonella y las células hospedadoras. SPI-1 promueve la invasión de Salmonella en las células epiteliales (16). El T3SS se ensambla a partir de las proteínas codificadas por SPI-1 y se denomina complejo aguja. Las translocasas y las proteínas efectoras se introducen en las células hospedadoras a través de este complejo, que abarca la envoltura bacteriana, y una extensión circular que sobresale de las membranas bacterianas interna y externa hacia las membranas de la célula hospedadora (17) (Figura 2). La Salmonella es absorbida por los macrófagos o las células dendríticas y transportada a través del sistema linfático hasta el bazo y el hígado (18-19).
La interacción generada entre la Salmonella Gallinarum y los macrófagos (MΦ) es la clave para la progresión de la infección sistémica de la Tifosis aviar porque la bacteria ha desarrollado sistemas de supervivencia dentro estas células denominado SPI-2 Tipo III (20-21). El sistema SPI-2 está compuesto por los plásmidos de virulencia necesarios para la persistencia de la infección sistémica que tienen un peso de 85kb, el cual inyecta sus moléculas efectoras en la célula huésped dentro de la vacuola fagocítica de los macrófagos (MΦ). Su principal efecto es interferir con el tráfico intracelular (Efecto fagocítico), impidiendo la fusión del fagosoma con los lisosomas (22). Mediante el análisis de hibridación de ADN se identificaron 42 marcos de lectura molecular u ORF que indicaron que solo un conjunto de estos genes era necesario para producir la infección sistémica de SG, y que codifican en el sistema de secreción tipo 3 (TTSS) del SPI-2 (23). La denominación molecular de esos factores de virulencia fue: aparato de secreción ssaU (aparato del sistema de secreción), los genes que codifican las proteínas sustrato tipo III y sus chaperonas específicas se denominaron sseP (sistema de secreción efector) y ssc (chaperona del sistema de secreción). Los genes que codifican las proteínas reguladoras de los genes de virulencia de SPI2 se denominaron ssr (regulador del sistema de secreción) (23). Jones et al. 2000 desafiaron aves de postura de tres semanas de edad con cepa de campo de Salmonella Gallinarum 9R y dos cepas mutantes que expresaran SPI-1 y SPI-2 para evaluar la invasión y la persistencia basado en los plásmidos ubicados en el SPI-1 (sseP-sistema de secreción efector) y SPI-2 (ssaU aparato del sistema de secreción) (24) (Figura 3).
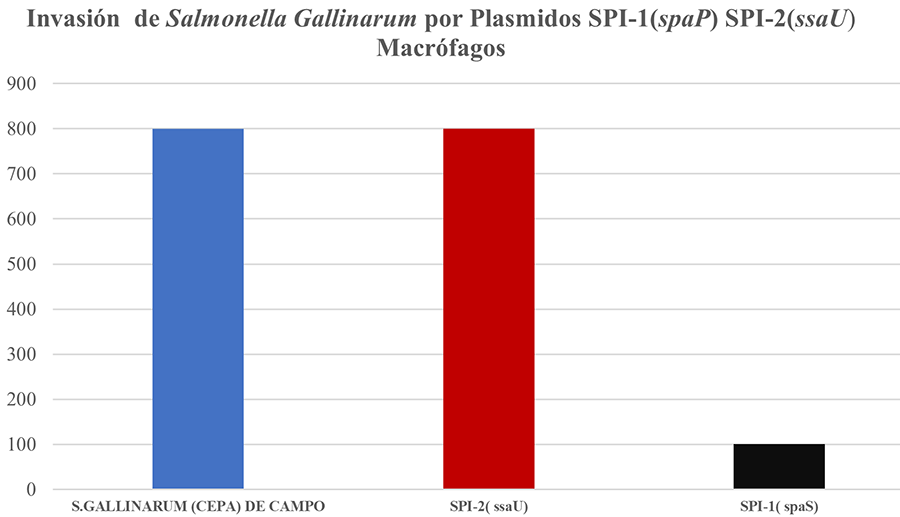

Los datos aquí presentados sugieren que, para que se produzca una invasión en los macrófagos por SG y se genere una infección sistémica, es necesario que se active fuertemente la molécula SPI-2 (ssaU). En contraste, se observa la baja activación del SPI-1(spaP) en los macrófagos que es la molécula necesaria para que se produzca una translocación vía sistema linfático hacia los órganos internos, especialmente el hígado y el bazo.
Se están empezando a dilucidar los mecanismos por los cuales SPI-2 actúa para promover la supervivencia dentro de los macrófagos. SPI-2 interfiere con el tráfico intracelular y participa en la inhibición de la maduración de los fagos lisosomas en macrófagos que contienen Salmonella. La función de SPI-2 también es necesaria para que la Salmonella intracelular evite ser eliminada por las especies reactivas del oxígeno (ROI). Esto parece lograrse mediante la exclusión de la fagocito oxidasa NADPH (Phox) de las vacuolas que contienen Salmonella (25). Las consecuencias de la activación de estos sistemas generan una distribución de las bacterias en el hígado, bazo, contenido de íleon y ciego. Luego de la infección oral con Salmonella Gallinarum 108, las cargas bacterianas a los 14 días post infección fueron reportadas como la media geométrica log10 CFU/gramo de tejido en hígado de cepa de campo 4.23, SPI-1(spaP) 4.38, SPI-2(ssaU) <1 y en bazo cepa de campo 4.23, SPI-1(spaP) 4.24, SPI-2(ssaU) <1 (24). Aunque hay poca diferencia en la biología de las interacciones entre serovares de Salmonella específicos del hospedador, en estudios que utilizan líneas celulares similares a los macrófagos aviares se reporta evidencia adicional de la importancia de la interacción entre la Salmonella-Macrófago (SAL-1– MΦ) que proviene de macrófagos primarios aislados de aves genéticamente resistentes y susceptibles (26) Los estudios in vivo han demostrado que las líneas endogámicas de White Leghorn muestran enormes diferencias en la susceptibilidad a la infección por S. Gallinarum (27), ya que los macrófagos de líneas resistentes a la SG expresan citocinas y quimiocinas más rápidamente y de mayor magnitud que las líneas de gallinas ponedoras susceptibles. Lo anterior sugiere que el sistema inmunológico se activa más rápidamente con mayor magnitud y de manera más efectiva en el proceso de fagocitosis para evitar el desarrollo de la infección sistémica (28). Con el objetivo de demostrar cuál es la velocidad y la magnitud de respuesta de los heterófilos a un desafío de Salmonella spp., Genovese et al. (1997) (29) reportó que al desafiar pollos vía intraperitoneal con Salmonella Enteritidis 5 x 104 a las 4 horas post infección, la invasión en el hígado fue del 83% del grupo control positivo vs 15% del grupo desafiado y tratado (p<0.001) y los heterófilos 0.9 x103/1mm3 del grupo control vs 5 x103/1mm3 del grupo desafiado y tratado (p<0.05), lo que demuestra que en un desafío por Salmonella la respuesta de la inmunidad celular es inmediata y es 5.1 veces superior.
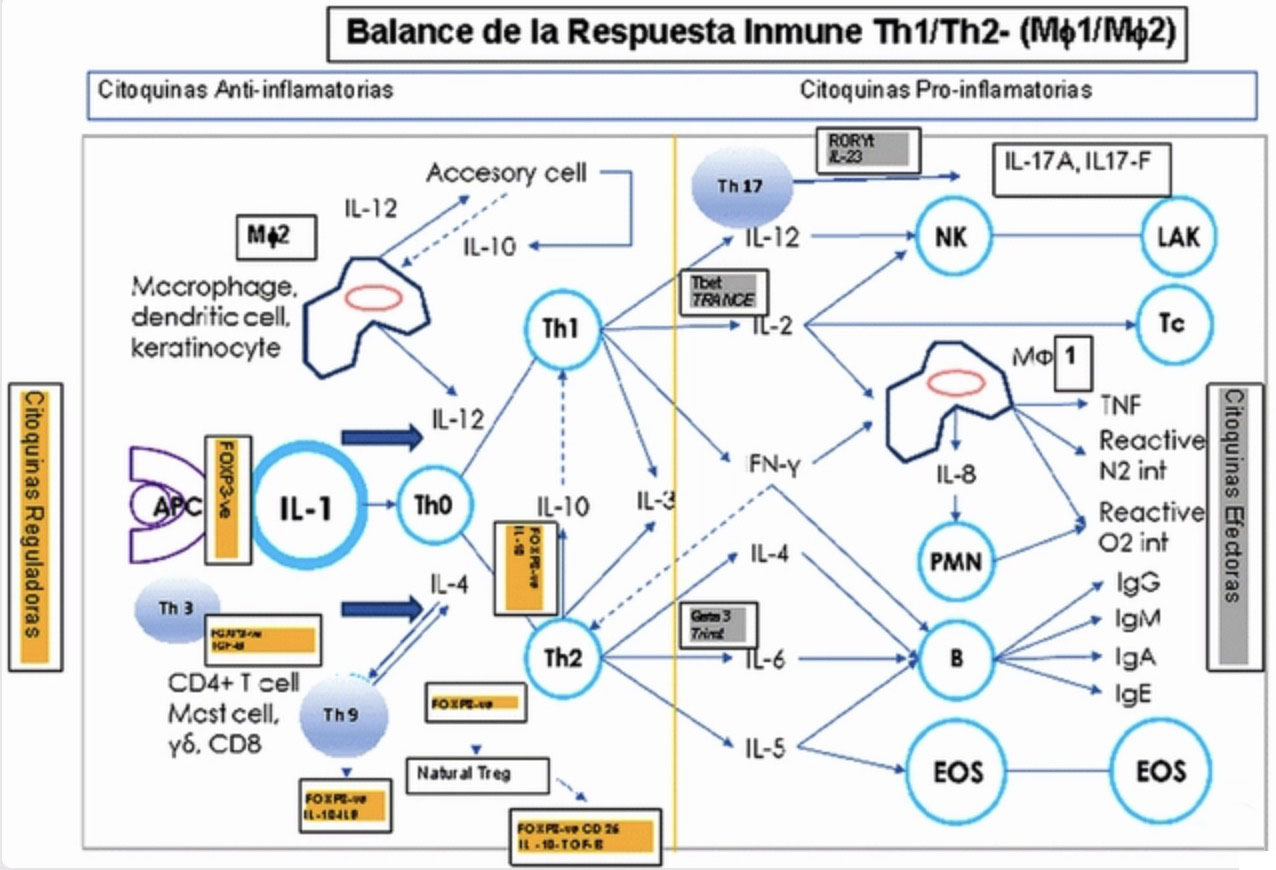
En respuesta a un desafío por Salmonella se produce un estímulo inicial de las quimiocinas CXCLi1 y CXCLi2 que provocan daño intestinal tres días después del desafío oral. Siete días después de la infección, esta respuesta disminuye y el daño inflamatorio se resuelve en gran medida posiblemente por el estímulo de los Th17 a pesar de la persistencia bacteriana (6). Recientemente, se ha demostrado la expresión de citocina IL-10 en las amígdalas cecales de aves infectadas con S. Enteritidis a los 4 días de la infección, pero no después de la infección con los serovares no inflamatorios adaptados a las aves (Figura 4) (6). Es probable que la regulación de las respuestas inmunitarias inflamatorias, presumiblemente por las células T reguladoras, permiten que la SG persista en el intestino durante varias semanas sin causar enfermedad al ave (6).
Las células CD4+ CD25+ de las aves producen citocinas de la familia IL-10 y TGF-β, y suprimen la proliferación de linfocitos Th in vitro. La estimulación de CD4+ CD25+ in vitro o in vivo con LPS (Lipopolisacáridos) de Salmonella, o con una infección, aumenta la actividad supresora. Curiosamente, también se ha demostrado que las CD4 +CD25+ se desplazan hacia la amígdala cecal, lo que sugiere que este órgano linfoide en la unión ileocecal podría desempeñar un papel clave en la regulación de la inmunidad intestinal (6).
La mayor evidencia científica para entender los mecanismos de inmunosupresión está en trabajos sobre la respuesta de las aves para eliminar la Salmonella Enteritidis y la Salmonella Typhimurium. La infección sistémica activa la IL-1β en respuesta a la hepatoesplenomegalia; evidentemente, cuando la bacteria ya se ha translocado a esos órganos (11). Sin embargo, para el efecto de la eliminación en el tubo gastrointestinal, la respuesta está dada por la expresión de la inmunidad celular tipo Th1 que se caracteriza por presentar altos niveles de la interleucina INF-γ entre los 14-28 días post-infección (31), que fortalece además la magnitud de la respuesta estimulando los macrófagos para que activen la fagocitosis en concomitancia con la expresión de la interleucina IL-8, IL-18 que generan una fuerte actividad pro inflamatoria (Figura 4) (31).
Una de las mayores dificultades para la eliminación de la Salmonella Gallinarum es su alta virulencia. Wigley et al., (2005) (32) evaluaron la respuesta inmune de la cepa vacunal 9R frente a un grupo de control negativo (sin vacuna) a las 3 semanas post infección. Los resultados confirman que entre la 3 o 4 semana post desafío, el nivel de IgG aumenta de 0.9 a 2.1 con Absorbancia de 490 nm vs el grupo control con un valor máximo de 0.5 Absorbancia de 490 nm (p<0.05). La proliferación de linfocitos T del grupo vacunado reportó una linfoproliferación de 9000 cpm vs el grupo control que fue de 2000 cpm (p<0.05). Además, se observó un aumento pronunciado del INF-γ que pasa de una carga de interleucinas de -2 a 8 (Ct) de la semana 2 a la semana 4 post infección (32). Lo anterior conduce a que la eliminación de la SG necesita ambos estímulos Th1 y Th2. La fase de infección inicial está dada por el estímulo de la inmunidad celular tipo Th1 que responde con un estímulo fuerte de alta producción de INF-γ y MΦ 1 que genere fagocitosis y, seguidamente, la alta expresión de IgG que genere una alta carga de anticuerpos modulada por la acción indirecta del INF-γ (Figura 4).
4. Fase 3: eliminación, persistencia y muerte
Luego del establecimiento de la SG por una infección sistémica, el ave puede controlar la replicación bacteriana y luego se convierte en un portador por la activación de la inmunidad adaptativa. Si la infección no es controlada por la inmunidad innata, Salmonella Gallinarum se replica en el bazo y en el hígado causando en estos órganos una fuerte hepatoesplenomegalia que causa además una anemia aplásica. El estado de una infección sistémica se produce cuando la SG se libera en una segunda cascada en el tracto gastrointestinal, causando hemorragia, inflamación y ulceración en la pared intestinal que conduce la muerte del ave en un periodo entre 6 a 10 días (30).
5. Fase 3: Respuesta inmune- Eliminación de S. Gallinarum
Dada la importancia de los linfocitos Th17 sobre la respuesta inflamatoria en los tejidos del tubo gastrointestinal, se hace necesario focalizar el análisis en las especies aviares. Estas se producen rápidamente luego de un desafío por Salmonella (6), posiblemente activadas por el estímulo de los TLR 5 que conduce a la expresión de Th 17. Esta a su vez estimula IL-17A e IL-17F que se producen con el objetivo de proteger la mucosa intestinal (Figura 4). En las ponedoras los Th17 aumentan su expresión en el ciego, que es el principal sitio de colonización por Salmonella Enteritidis (6).
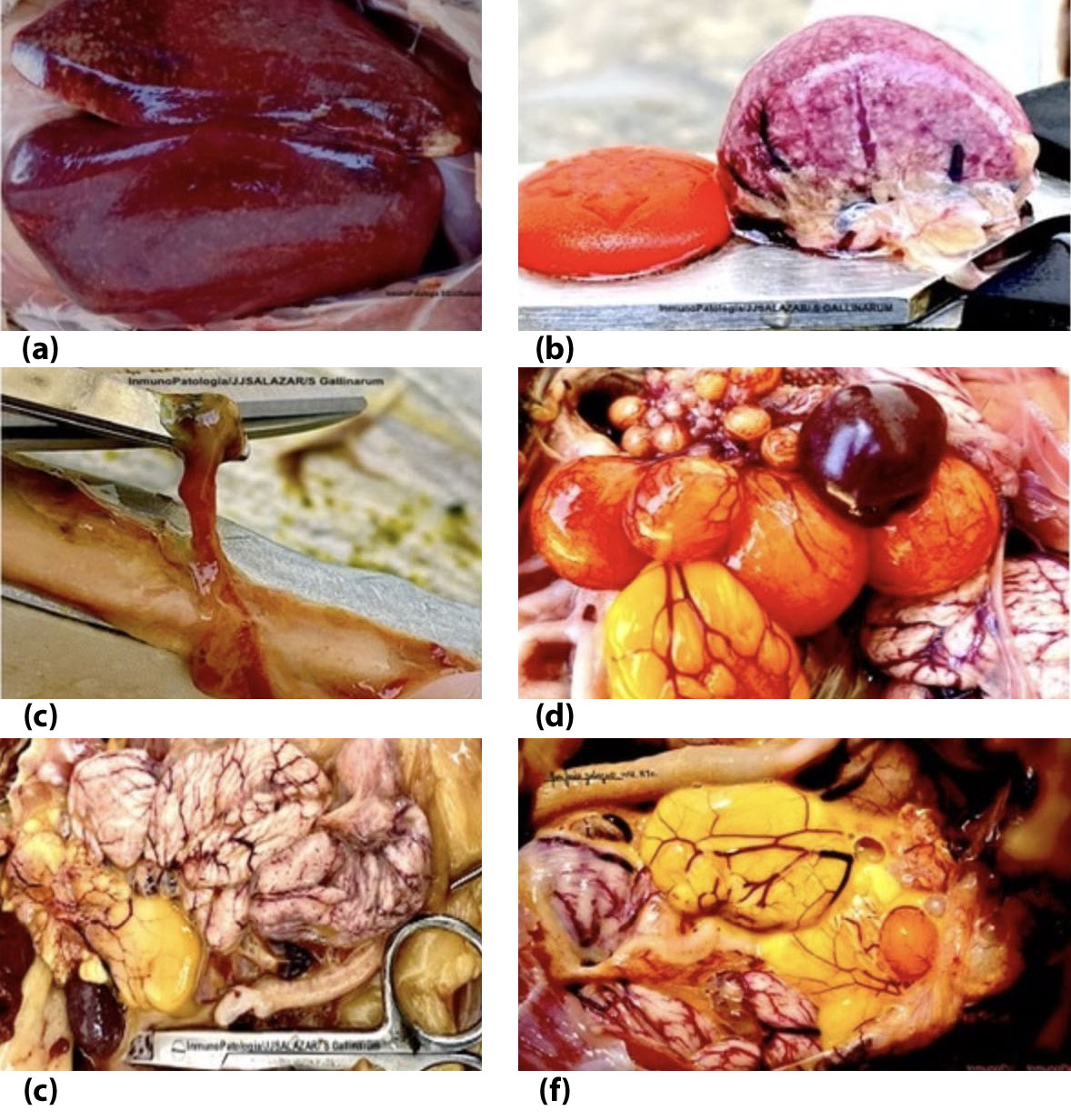
6. Fase 3: bases inmunológicas del estado de portador(persistencia) e inmunosupresión por disminución de CD4+ en pico de producción por efecto de madurez sexual.
La persistencia de la Salmonella Gallinarum y la Salmonella Pullorum frente a la respuesta de la inmunidad celular y humoral es un cuestionamiento biológico muy interesante, especialmente sobre la transmisión a los huevos. Solo por el hecho de quedarse dentro de los fagolisosomas de los macrófagos del bazo e hígado, habilitando las posibilidades genéticas que le brinda el sistema SPI-2 que evita la fagocitosis y permite la persistencia de la SG. En las ponedoras comerciales que están comenzando la madurez sexual y que son desafiadas con SG se puede presentar un recrudecimiento de la infección al inicio de la postura; esto está relacionado con la expresión fisiológica y hormonal del ave (33). Por lo tanto, la persistencia durante el resto de la vida del ave positiva a cepas de campo se mantiene por la expresión del SPI-2 a través de la regulación negativa del CMH (Complejo Mayor de Histocompatibilidad) en la superficie celular que desencadena la expresión de la IL-10 que es una molécula antiinflamatoria que promueve la inmunosupresión (34).
Chapel et al. (2009) (11) compararon la respuesta de la inmunidad celular Th1 con la inmunidad humoral Th2 al evaluar la expresión de INF-γ, IL-18-, IL-4 en aves desafiadas con Salmonella Enteritidis y Salmonella Pullorum en aves desafiadas a los 14 días post infección con el objetivo de estudiar la persistencia dentro de los macrófagos y realizar un análisis de la prospectiva de la producción de anticuerpos (Figura 4-5).
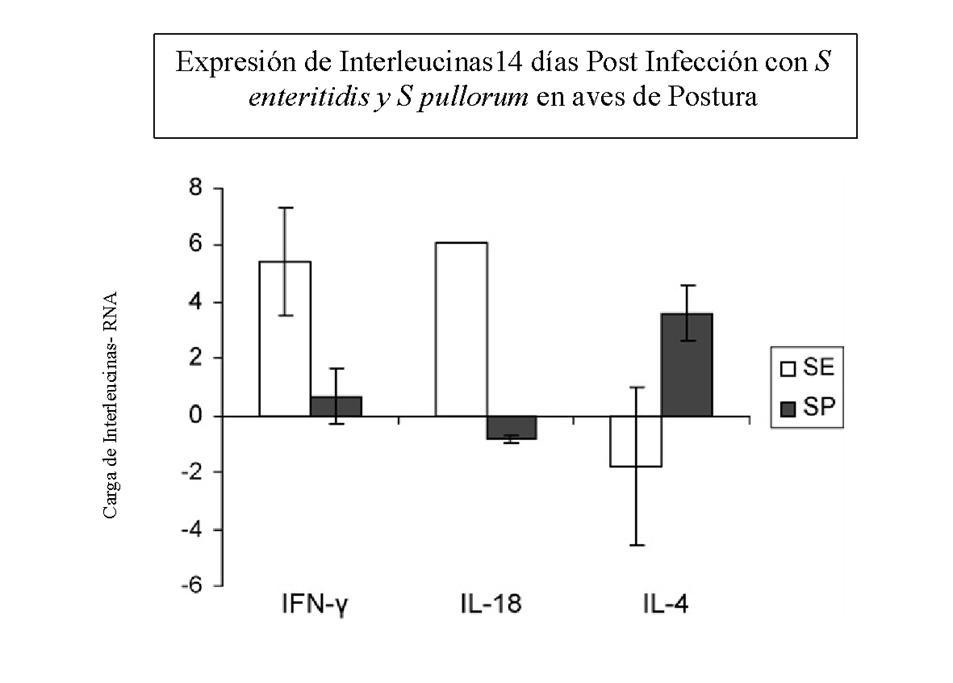
En las aves desafiadas con S. Enteritidis se presentó en aumento significativo de la respuesta de las interleucinas IFN-γ, IL-18 demostrando la asociación causal de los Th1 comparados con la IL-4 que reportan valores muy bajos y que está relacionada con la expresión de Th2 (p=0.045). De forma contraria se observa que en las aves desafiadas con S. Pullorum, la expresión de IFN-γ, IL-18 presentó cargas muy bajas o negativas, y que la IL-4 reportó cargas altas, indicando que la respuesta inmune en los desafíos por salmonelas tíficas depende de la inmunidad humoral Th2 principalmente (11). De igual manera, se observó que la cantidad de bacterias de S. Enteritidis evaluada a los 28 días, en los macrófagos del bazo se eliminaron totalmente debido a la alta expresión de IFN-γ, pero no en las aves desafiadas con S. Pullorum donde la carga se mantiene a los 28 días post infección con un valor promedio de 2 log10. Esto refleja la diferencia entre la respuesta Th1 y Th2 que se debe principalmente a la persistencia de las salmonellas tíficas (S. Pullorum, S. Gallinarum) dentro de los macrófagos y la incapacidad de ser eliminadas debido a la fuerte activación de su virulencia en su SPI-2 (ssaU aparato del sistema de secreción) (11). Por último, es posible que se presente una falla en la función proliferativa de los linfocitos CD4+ generando una cantidad reducida de estas células causando un estado de inmunosupresión especialmente en las células del tracto reproductivo cuando comienza el pico de producción (35).
Conclusiones
La infección por Salmonella Gallinarum y la activación del sistema inmune es un punto de gran interés para comprender las diferencias entre la inmunidad de tipo celular (Th1) y la de tipo humoral (Th2). Estas diferencias demuestran que hay tres fases de infección para lograr su control. En la primera fase (Invasión gastrointestinal) la cantidad de la carga bacteriana es una variable crítica porque en un desafío fuerte se produce la lesión de los enterocitos que la bacteria aprovecha activando el sistema de evasión SPI-1 para lograr translocar a la circulación sistémica, y contaminar el hígado y el bazo. En intestino el ave responde activando la secreción de las moléculas proinflamatorias CXCLi1 y CXCLi2 y donde la respuesta es muy baja frente a la respuesta del CXCLi1 por S. Gallinarum. Por lo tanto, la respuesta inmune de tipo celular es muy deficiente para lograr un control en el lumen intestinal que depende de la carga de la bacteria.
En la segunda fase de infección sistémica, la bacteria se transloca al hígado y al bazo, activando el sistema de evasión SPI-2 donde la respuesta inmune se ve afectada para activar los Macrófagos y su función más importante la fagocitosis. Es en este momento que SG activa los genes expresados por el SPI-2 evitando la activación de los fagolisosomas y bloqueando su eliminación. En este punto hay que facilitarle al ave la posibilidad de que el sistema inmune exprese altas cargas de IFN-γ para controlarla mediante la respuesta de la inmunidad humoral ; lo que se logra estimulando al ave con la aplicación de vacunas SG-9R con dos dosis en la etapa de levante(Primo-vacunación entre 6-8 semanas y refuerzo entre la 14-16 semana) Igualmente que al usar la cepas de vacunas vivas de Salmonella Enteritidis que está basada en la cepa mutante Ssq/Sm24/Rif12 con deriva metabólica en un programa de tres dosis en las semanas 1, 6, 16 con refuerzos a la semana 60 vía agua de bebida.
Por último, en la tercera fase se genera alta mortalidad y persistencia por disminución de la de fagocitosis en los macrófagos y baja cargas de IFN-γ; el sistema SPI-2 activa fuertemente la secreción de IL-10 que actúa como una molécula antiinflamatoria, la cual bloquea la respuesta inmune de tipo humoral. Esto conduce a una baja producción de CD4+ en su maduración y proliferación generando en los lotes afectados un estado de inmunosupresión constante. El análisis de la inmunobiología demuestra que cuando Salmonella Gallinarum para su estado de persistencia depende fuertemente de la Inmunidad mediada principalmente por la inmunidad humoral, mientras que en S. Enteritidis depende fuertemente de la respuesta brindada por la inmunidad celular.
Es necesario entender el papel de la microbiota en el desarrollo y la homeostasis del sistema inmunitario del ave, que requiere mejorar nuestra comprensión sobre los mecanismos fundamentales sobre la respuesta inmune. Si bien el objetivo final del inmunólogo es mejorar los programas de vacunación y otros controles que reduzcan la carga de Salmonella spp., también debe argumentar claramente la comprensión de las implicaciones para la salud de las aves. Argumento que es cada vez más importante para el consumidor final cuando entienden la causa de resistencias a los antibióticos que se pueden transmitir a los seres humanos.
2. Recomendaciones prácticas para el control de la Salmonella en campo
La reducción de Salmonella en las granjas es un paso muy importante, para lo cual hay que implementar un plan holístico de disminución de la infección. 1) Es necesario usar un programa de limpieza y desinfección efectivo contra Salmonella spp., ya que se ha demostrado que persiste por más de 15 meses en el ambiente en techos, jaulas, cintas transportadoras, huevos, comederos, ventiladores, polvo. Otro factor crucial de cualquier estrategia de control es la prevención de la contaminación del alimento. 2) Se ha propuesto hacer intervenciones sobre la dieta alimenticia para evitar la disbacteriosis, ya que la microbiota intestinal tiene un impacto en el huésped incluyendo cómo se modula el sistema inmunológico, cómo se descomponen los nutrientes y cómo se controlan la funciones intestinales, lo que se puede fortalecer con el uso de prebióticos, probióticos, simbióticos, ácidos grasos de cadena media (MCFA), ácido caprico, caproico y caprílico y otros ácidos como el fórmico y acético. 3) uso de vacunas en programas de control y erradicación. El argumento más fuerte de esta revisión sistemática es que la Salmonella Gallinarum requiere para su control en su mayor parte del estímulo de la inmunidad humoral (Linfocitos Th2) que es generado por un antígeno vacunal, para lo cual la industria colombiana permite el uso de la vacuna SG-9R (bajo el concepto de autorización del uso de emergencia) con dos dosis en la etapa de levante (primo vacunación entre 6-8 semanas y refuerzo entre la 14-16 semanas). Igualmente, la ciencia ha demostrado que al usar las cepas de vacunas vivas de Salmonella Enteritidis que están basada en la cepa mutante Ssq/Sm24/Rif12 con deriva metabólica se controlan las infecciones por Salmonella Gallinarum al generar PROTECCIÓN CRUZADA por poseer los serotipos del mismo grupo antigénico O 9 (D1) con programas en el levante a 1 semana (vacuna viva en agua), 6 semanas (vacuna viva en agua) y 16 semanas (vacuna oleosa) con revacunaciones en agua de bebida a la semana 60 de vida.
Referencias
- Barrow PA. The paratyphoid salmonellae. Rev Sci Tech. 2000;19:351–375.
- Shivaprasad HL. Fowl typhoid and pullorum disease. Rev Sci Tech. 2000;19:405–424.
- Jones MA, Wigley P, Page KL, Hulme SD, Barrow PA. Salmonella enterica serovar Gallinarum requires the Salmonella pathogenicity island 2 type III secretion system but not the Salmonella pathogenicity island 1 type III secretion system for virulence in chickens. Infect Immun. 2001;69:5471–5476.
- Parmar D, Davies R. Fowl typhoid in a small backyard laying flock. Vet Rec. 2007;160:348.
- Chacón RD, Moura Q, Astolfi-Ferreira CS, De la Torre DI, Guerrero LMC, Martínez LAR, et al. Draft genome sequences of four Salmonella enterica subsp. enterica serovar Gallinarum strains isolated from layer breeder flocks in an outbreak of fowl typhoid in Colombia. Microbiol Resour Announc. 2019;8:e00122-19. https://doi.org/10.1128/MRA.00122-19
- Wigley P. Salmonella enterica in the chicken: how it has helped our understanding of immunology in a non-biomedical model species. Front Immunol. 2014;5:482. doi:10.3389/fimmu.2014.00482
- Smith AL, Beal R. The avian enteric immune system in health and disease. In: Davison F, Kaspers B, Schat KA, editors. Avian Immunology. London: Academic Press; 2008. p. 243–271.
- Withanage GS, Wigley P, Kaiser P, Mastroeni P, Brooks H, Powers C, et al. Cytokine and chemokine responses associated with clearance of a primary Salmonella entérica serovar Typhimurium infection in the chicken and in protective immunity to rechallenge. Infect Immun. 2005;73:5173–5182.
- Henderson SC, Bounous DI, Lee MD. Early events in the pathogenesis of avian salmonellosis. Infect Immun. 1999;67:3580–3586.
- Withanage GS, Kaiser P, Wigley P, Powers C, Mastroeni P, Brooks H, et al. Rapid expression of chemokines and proinflammatory cytokines in newly hatched chickens infected with Salmonella entérica serovar Typhimurium. Infect Immun. 2004;72:2152–2159.
- Chappell L, Kaiser P, Barrow P, Jones M, Claire P, Wigley P. The immunobiology of avian systemic salmonellosis. Vet Immunol Immunopathol. 2009;128:53–59. doi:10.1016/j.vetimm.2008.10.295
- Kaiser P, Rothwell L, Galyov EE, Barrow PA, Burnside J, Wigley P. Differential cytokine expression in avian cells in response to invasion by Salmonella typhimurium, Salmonella enteritidis and Salmonella gallinarum. Microbiology. 2000;146(Pt 12):3217–3226.
- Rojas W, et al. Inmunología de Rojas. Elementos constitutivos, barreras naturales, células, moléculas y sistemas enzimáticos de la inmunidad innata. 2023;19:24–25.
- Iqbal M, Philbin VJ, Withanage GS, Wigley P, Beal RK, Goodchild MJ, et al. Identification and functional characterization of chicken toll-like receptor 5 reveals a fundamental role in the biology of infection with Salmonella entérica serovar Typhimurium. Infect Immun. 2005;73:2344–2350.
- Hansen-Wester I, Hensel M. Salmonella pathogenicity islands encoding type III secretion systems. Microbes Infect. 2001;3:549–559. doi:10.1016/S1286-4579(01)01411-3
- Raffatellu M, Wilson RP, Chessa D, Andrews-Polymenis H, Tran QT, Lawhon S, et al. SipA, SopA, SopB, SopD, and SopE2 contribute to Salmonella entérica serotype Typhimurium invasion of epithelial cells. Infect Immun. 2005;73:146–154. doi:10.1128/IAI.73.1.146-154.2005
- Kubori T, Matsushima Y, Nakamura D, Uralil J, Lara-Tejero M, Sukhan A, et al. Supramolecular structure of the Salmonella typhimurium type III protein secretion system. Science. 1998;280:602–605. doi:10.1126/science.280.5363.602
- Mastroeni P, Menager N. Development of acquired immunity to Salmonella. J Med Microbiol. 2003;52:453–459.
- Lou L, Zhang P, Piao R, Wang Y. Salmonella pathogenicity island 1 (SPI-1) and its complex regulatory network. Front Cell Infect Microbiol. 2019;9:270. doi:10.3389/fcimb.2019.00270
- Barrow PA. The paratyphoid salmonella. Rev Sci Tech. 2000;19:351–375.
- Hensel M. Salmonella pathogenicity island 2. Mol Microbiol. 2000;36:1015–1023.
- Cheminay C, Mohlenbrink A, Hensel M. Intracellular Salmonella inhibit antigen presentation by dendritic cells. J Immunol. 2005;174:2892–2899.
- Hensel M, et al. Salmonella pathogenicity island 2. Mol Microbiol. 2000;36(5):1015–1023.
- Jones M, Wigley W, Kerrel L, Sott DH, Hums (dato faltante), Barrow P. Salmonella enterica serovar Gallinarum requires the Salmonella pathogenicity island 2 type III secretion system but not the Salmonella pathogenicity island 1 type III secretion system for virulence in chickens. Infect Immun. 2000;69:5471–5476. doi:10.1128/IAI.69.9.5471–5476.200
- Vazquez-Torres A, Jones-Carson J, Mastroeni P, Ischiropoulos H, Fang FC. Antimicrobial actions of the NADPH phagocyte oxidase and inducible nitric oxide synthase in experimental salmonellosis. I. Effects on microbial killing by activated peritoneal macrophages in vitro. J Exp Med. 2000;192:227–236.
- Wigley P. Genetic resistance to Salmonella infection in domestic animals. Res Vet Sci. 2004;76:165–169.
- Wigley P, Hulme SD, Bumstead N, Barrow PA. In vivo and in vitro studies of genetic resistance to systemic salmonellosis in the chicken encoded by the SAL1 locus. Microbes Infect. 2002;4:1111–1120.
- Wigley P, Hulme S, Rothwell L, Bumstead N, Kaiser P, Barrow P. Macrophages isolated from chickens genetically resistant or susceptible to systemic salmonellosis show magnitudinal and temporal differential expression of cytokines and chemokines following Salmonella enterica challenge. Infect Immun. 2006;74:1425–1430.
- Genovese KJ, Kogut H. Resistance of Salmonella enteritidis invasion organs in day-old turkey and chickens by transformed cell T produce lymphokines. Avian Dis. 1997;42:545–553.
- Shivaprasad HL. Fowl typhoid and pullorum disease. Rev Sci Tech. 2000;19:405–424.
- Babu U, Scott M, Myers MJ, Okamura M, Gaines D, Yancy HF, et al. Effects of live attenuated and killed Salmonella vaccine on T-lymphocyte mediated immunity in laying hens. Vet Immunol Immunopathol. 2003;91:39–44.
- Wigley P, Hulme S, Powers C, Beal R, Smith A, Barrow P. Oral infection with the Salmonella enterica serovar Gallinarum 9R attenuated live vaccine as a model to characterise immunity to fowl typhoid in the chicken. BMC Vet Res. 2005;1:2.
- Wigley P, Hulme SD, Powers C, Beal RK, Berchieri A Jr, Smith A, Barrow P. Infection of the reproductive tract and eggs with Salmonella enterica serovar Pullorum in the chicken is associated with suppression of cellular immunity at sexual maturity. Infect Immun. 2005;73:2986–2990.
- Uchiya K, Groisman EA, Nikai T. Involvement of Salmonella pathogenicity island 2 in the up-regulation of interleukin-10 expression in macrophages: role of protein kinase A signal pathway. Infect Immun. 2004;72:1964–1973.
- Johnston CE, Hartley C, Salisbury AM, Wigley P. Immunological changes at point-of-lay increase susceptibility to Salmonella enterica serovar Enteritidis infection in vaccinated chickens. PLoS One. 2012;7:e48195. doi:10.1371/journal.pone.0048195
John Jairo Salazar. MVZ. MSc. Esp1
1. Director Avicultura Latam
InmunoPatología Amerivet SAS
Jsalazar@amerivet.co
johnjairo.salazar@gmail.com.