Introducción
En los sistemas modernos de producción avícola, la salud intestinal se ha convertido en un pilar clave para garantizar la sanidad, el bienestar y el rendimiento productivo de las aves. Un tracto gastrointestinal funcional no solo es esencial para una adecuada digestión y absorción de nutrientes, sino que también cumple un rol fundamental como barrera física, inmunológica y microbiológica frente a patógenos y toxinas del ambiente. La eficiencia alimenticia, el crecimiento y la conversión son altamente dependientes de un equilibrio intestinal estable, especialmente bajo condiciones de alta densidad, restricciones sanitarias y presión productiva (1).
Además de su función digestiva, el intestino actúa como el principal punto de interacción entre el organismo y el medio externo, convirtiéndose en una estructura crítica en la prevención de enfermedades sistémicas. Alteraciones en la microbiota, inflamación intestinal, o disfunción en la barrera epitelial pueden facilitar la translocación de bacterias o sus componentes hacia la circulación, con posibles repercusiones en órganos extraintestinales. En este contexto, el mantenimiento de la integridad intestinal no solo es una estrategia de salud, sino un componente indispensable de la sostenibilidad y eficiencia de la producción avícola moderna (2-4).

Entendiendo el concepto de salud intestinal
La salud intestinal óptima es de vital importancia para el rendimiento de los animales de producción. En las industrias pecuarias, el concepto de salud intestinal es prácticamente sinónimo de salud general del animal. No obstante, no existe una definición ampliamente aceptada y estandarizada de “salud intestinal” (5).
Según la definición propuesta por la Organización Mundial de la Salud (OMS) en 1948 la salud se entiende como “un estado de completo bienestar físico, mental y social, y no solamente la ausencia de afecciones o enfermedades”. A partir de esta visión positiva del concepto de salud, Bischoff en 2011 definió la salud intestinal como “un estado de bienestar físico y mental en ausencia de molestias gastrointestinales que requieran consulta médica, sin indicios ni riesgos de enfermedades intestinales, y en ausencia de enfermedad intestinal confirmada” (5). Aunque esta definición se refiere específicamente a la salud humana, Bischoff argumenta que la prevención o evitación de enfermedades gastrointestinales forma parte integral de nuestra comprensión general del concepto de salud, siendo a su vez estos conceptos aplicables a la medicina veterinaria y a los sistemas de producción de proteína animal (6).
En concordancia y aportando en el entendimiento del concepto, Kogut y Arsenault definieron la salud intestinal como la “ausencia, prevención o evitación de enfermedades, de modo que el animal sea capaz de llevar a cabo sus funciones fisiológicas y resistir estresores exógenos y endógenos” (7), Esta definición funcional puede integrarse a su vez con los cinco criterios fundamentales propuestos por Bischoff como base para una definición abarcadora de salud intestinal (5):
- Digestión y absorción eficaces de los alimentos.
- Ausencia de enfermedades gastrointestinales.
- Microbioma intestinal normal y estable.
- Estado inmunológico eficaz.
- Estado general de bienestar.
Posteriormente, Celi et al. ampliaron este enfoque, señalando que los componentes clave de la funcionalidad del tracto gastrointestinal (TGI) incluyen (8):
- Una estructura y función eficaces de la barrera gastrointestinal.
- La interacción adecuada entre el huésped y la microbiota intestinal.
- Una digestión y absorción de nutrientes efectivas.
- Un sistema inmunológico competente.
De esta manera, aunque no existe aún una definición unificada de “salud intestinal”, existe un consenso creciente sobre su papel fundamental en la productividad animal. A medida que avanza el conocimiento sobre los componentes intestinales y sus interacciones con la dieta, el ambiente y los microorganismos, el concepto de salud intestinal se vuelve más complejo y dinámico. En la actualidad, como lo mencionan diversos autores, la salud intestinal debe entenderse como una condición general de homeostasis del TGI, tanto en su estructura como en su función, y no simplemente como la ausencia de enfermedad, ya sea clínica o subclínica (6).
¿Cómo funciona la barrera intestinal?
Dentro del concepto de salud intestinal, se ha resaltado como una de las funciones clave del epitelio intestinal su capacidad para digerir y absorber los nutrientes presentes en los alimentos. No obstante, un intestino “saludable” cumple un papel que va mucho más allá, al involucrar múltiples funciones. Entre ellas, destaca su función estructural y de barrera, mediante la cual el epitelio actúa como una barrera física y bioquímica, destinada a impedir la difusión de patógenos, toxinas y alérgenos desde la luz del TGI hacia la circulación sistémica y los tejidos circundantes (9). Esta barrera intestinal es un sistema complejo y dinámico que depende de la interacción de varios componentes que incluyen principalmente:
- Moco
- Inmunoglobulina A
- Péptidos antimicrobianos
- Microbiota
- Células inmunitarias
- Uniones estrechas
Se ha descrito que los componentes de la barrera intestinal están organizados en tres capas interactivas las cuales, descritas en orden desde la luz hacia la mucosa, corresponden a una primera capa compuesta por la microbiota comensal del hospedador, la cual, mediante mecanismos como la exclusión competitiva, la producción de metabolitos antimicrobianos y la modulación del entorno luminal, contribuye a inhibir la colonización por bacterias potencialmente patógenas (10-11).
La segunda capa está compuesta por el moco intestinal, una matriz secretada por células caliciformes intestinales que se mezcla con moléculas con acción antimicrobianas como la IgA y péptidos como la lisozima y las defensinas producidas principalmente por células de Paneth, enterocitos y células del sistema inmunológico. Esta capa actúa como una barrera química y física dinámica, que regula la interacción entre la microbiota y el epitelio subyacente, contribuyendo a que microorganismos patógenos no alcancen a unirse a la mucosa intestinal (11).
Finalmente, la tercera capa de la barrera intestinal está constituida por el epitelio intestinal, en el que los enterocitos están conectados entre sí por medio de complejos de uniones intercelulares, incluyendo las uniones estrechas (tight junctions), las uniones adherentes y los desmosomas. Estas estructuras permiten regular el transporte paracelular y son fundamentales para la función de barrera epitelial. Cabe destacar que, por debajo de esta capa epitelial, la lámina propia alberga un componente inmunológico especializado, conformado por células del sistema inmune innato y adaptativo, tales como células dendríticas, linfocitos B, linfocitos T y macrófagos, que fortalecen la defensa frente a antígenos y patógenos (11).
Las uniones estrechas como parte de la barrera intestinal
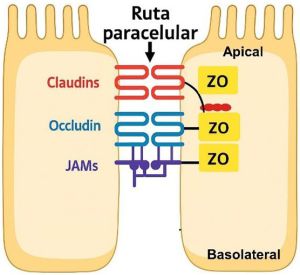
Dentro del concepto integrado de la barrera intestinal como un conjunto de mecanismos de protección en los animales, las uniones estrechas se consideran el principal componente de la barrera física del intestino. Estas estructuras, conocidas como uniones estrechas, están formadas por un entramado de proteínas ensambladas en la porción apical de la membrana lateral de las células epiteliales, y su función es permitir el paso selectivo de compuestos a través de las rutas paracelulares (es decir, entre las células) (Figura 1). Esta estructura incluye proteínas transmembrana como la claudina (CL), la ocludina (OC) y la molécula de adhesión de unión A (JAM-A), así como proteínas del entramado intracelular como la zónula ocludens (ZO). Visto desde una perspectiva estructural y funcional, las proteínas ZO actúan como anclajes intracelulares que conectan a las proteínas transmembrana (CL, OC y JAM-A) con el citoesqueleto de las células intestinales para regular el cierre de la barrera (9).
Translocación bacteriana y sanidad avícola
Es importante destacar que un aumento en la permeabilidad intestinal no conduce necesariamente a una mayor translocación bacteriana a través de vías paracelulares. Sin embargo, múltiples estudios han reportado que marcadores como Lactulosa/Manitol o el dextrano conjugado con isotiocianato de fluoresceína (FITC-d), con un peso molecular de 3,000 a 5,000 Da, pueden pasar desde la luz intestinal al torrente sanguíneo (Figura 2). A pesar de ello, la patogénesis exacta del paso de bacterias, toxinas o moléculas como FITC-d hacia la circulación sistémica y órganos internos como el hígado no ha sido completamente elucidada y continúa siendo objeto de investigación (3, 13).
En este sentido, diversos estudios han profundizado en la importancia de la barrera intestinal como determinante clave para la aparición de enfermedades óseas en las aves, como la condronecrosis bacteriana con osteomielitis (BCO) en pollos de engorde. Factores como disbiosis, estrés o daño a las uniones estrechas del epitelio intestinal pueden aumentar la permeabilidad intestinal y facilitar la translocación de bacterias hacia la sangre. Estas bacterias, al distribuirse por vía hematógena, pueden colonizar microfracturas en las placas de crecimiento de huesos largos, generando lesiones típicas de BCO. Esta conexión entre intestino y hueso se refuerza por estudios que muestran una reducción en la incidencia de cojeras mediante el uso de aditivos que mejoran la salud intestinal, lo que ayuda a reforzar la idea de que el TGI actúa como puerta de entrada crítica para infecciones óseas de origen bacteriano (21-22).
Por otra parte, el hígado ha sido otro blanco de estudio referente a la translocación bacteriana, esto debido a que la mayor parte del drenaje venoso del tracto gastrointestinal fluye hacia la circulación portal; el hígado es el primer órgano en entrar en contacto con nutrientes, toxinas o bacterias derivadas del intestino. En este contexto, el estudio de Baxter et al. (23), reportó la asociación entre el aumento en la permeabilidad intestinal, evaluada mediante niveles séricos de FITC-d, y la presencia de bacterias viables en hígado, donde aves alimentadas con dietas ricas en centeno con mayor viscosidad fecal mostraron tanto un incremento significativo de FITC-d en suero como un mayor recuento de unidades formadoras de colonias en tejido hepático. Sugiriendo así, que daños en la integridad de la barrera paracelular intestinal, puede facilitar ingreso de bacterias hacia la circulación portal con impacto sobre órganos extraintestinales (23).

No solo las bacterias viables pueden translocarse desde el intestino, sino también componentes bacterianos como el lipopolisacárido (LPS), una endotoxina presente en la membrana externa de bacterias gramnegativas capaz de inducir estímulos de tipo proinflamatorios. En un modelo de gota visceral en gansos, Xi et al. demostraron que la disbiosis intestinal y el aumento en la permeabilidad epitelial, evidenciado por la disminución en la expresión de proteínas de uniones estrechas (OC, ZO, CL), permitieron el paso de LPS al torrente sanguíneo, lo cual activó rutas de respuestas inflamatorias sistémicas. Además, se observó una correlación positiva entre los niveles séricos de LPS y biomarcadores de daño renal, lo que sugiere que la translocación de productos bacterianos puede contribuir directamente al desarrollo de lesiones inflamatorias en órganos extraintestinales como el caso del riñón en los gansos (24).
En conjunto, estos hallazgos refuerzan el papel clave de la barrera intestinal como eje integrador entre la microbiota, el sistema inmune y la salud sistémica en aves. Más allá de actuar como un filtro físico, su integridad determina la exposición del organismo a bacterias y productos bacterianos como el LPS, capaces de desencadenar problemas en órganos distantes como el hígado, el riñón o incluso el tejido óseo. Esta problemática de permeabilidad intestinal ya es sabido que puede verse agravada por problemas de disbiosis, enteritis, estrés térmico o problemas nutricionales representa un factor crítico en la fisiopatología de múltiples enfermedades tanto intestinales como sistémicas (2). En este contexto, la evaluación de la permeabilidad intestinal mediante herramientas como FITC-dextrano ofrece una vía experimental valiosa para anticipar el riesgo de translocación bacteriana y su impacto en la salud sistémica de los lotes de aves. Por tanto, proteger la barrera intestinal se perfila como una estrategia fundamental en la prevención de enfermedades inflamatorias de origen entérico en la avicultura moderna (23).

Recomendaciones
Dado el alto nivel de exigencia productiva en la avicultura moderna, se vuelve indispensable para veterinarios y nutricionistas adoptar un enfoque integral que tenga en cuenta la salud y barrera intestinal como eje fundamental del rendimiento zootécnico y sanitario. En este contexto, se proponen tres recomendaciones clave:
Implementación de programas integrales de monitoreo intestinal, que incluyan evaluaciones macro y microscópicas de la mucosa, diagnóstico sistemático de patógenos como Eimeria spp. Adicionalmente, es recomendable comenzar a implementar pruebas de permeabilidad en campo como puede ser el FITC-dextran, el cual actualmente es el método más validado para detectar alteraciones subclínicas de la barrera intestinal.
Optimizar las condiciones de manejo, controlando factores como la temperatura, densidad, ventilación y limpieza, con el objetivo de minimizar el estrés ambiental y preservar la homeostasis intestinal y con ello el estado de la barrera.
Inclusión estratégica de aditivos moduladores de la salud intestinal, como aceites esenciales, prebióticos, probióticos, entre otros, que fortalezcan la mucosa y regulen estados de inflamación de manera que promuevan una barrera intestinal más funcional.
Conclusión
La evidencia revisada respalda firmemente que la integridad de la barrera intestinal en aves es un factor determinante para la salud sistémica y la productividad en los sistemas avícolas modernos. Alteraciones en la microbiota, dietas proinflamatorias, infecciones entéricas o estrés ambiental pueden comprometer esta barrera, permitiendo la translocación de bacterias viables o de componentes como el LPS hacia órganos internos, especialmente el hígado. Este proceso no solo agrava cuadros locales de enteritis, sino que también puede originar patologías extraintestinales, como la osteomielitis bacteriana o la inflamación hepática. En este sentido, la barrera intestinal cumple un rol esencial y silencioso en la protección del ave, evitando la entrada sistémica de microorganismos. Sin embargo, cuando se presentan alteraciones inflamatorias, infecciosas o desequilibrios en la salud intestinal, se incrementa la permeabilidad epitelial, lo cual puede repercutir negativamente en la sanidad general del ave. Por tanto, preservar la salud intestinal e implementar herramientas de monitoreo de la integridad epitelial y la permeabilidad resulta fundamental para asegurar la eficiencia productiva y el bienestar animal en la avicultura moderna.
Referencias
- Ducatelle R, Goossens E, Eeckhaut V, Van Immerseel F. Poultry gut health and beyond. Anim Nutr. 2023;13:240–248. https://doi.org/10.1016/j.aninu.2023.03.005
- Abdelhamid MK, Quijada NM, Dzieciol M, Hatfaludi T, Bilic I, Selberherr E, et al. Co-infection of chicken layers with Histomonas meleagridis and avian pathogenic Escherichia coli is associated with dysbiosis, cecal colonization and translocation of the bacteria from the gut lumen. Front Microbiol. 2020;11. https://doi.org/10.3389/fmicb.2020.586437
- Gilani S, Chrystal PV, Barekatain R. Current experimental models, assessment and dietary modulations of intestinal permeability in broiler chickens. Anim Nutr. 2021;7(3):801–811. https://doi.org/10.1016/j.aninu.2021.03.001
- Wells JM, Brummer RJ, Derrien M, MacDonald TT, Troost F, Cani PD, et al. Homeostasis of the gut barrier and potential biomarkers. Am J Physiol Gastrointest Liver Physiol. 2017;312(3):G171–G193. https://doi.org/10.1152/ajpgi.00048.2015
- Bischoff SC. “Gut health”: a new objective in medicine? BMC Med. 2011;9(1):24. https://doi.org/10.1186/1741-7015-9-24
- Pluske JR, Turpin DL, Kim JC. Gastrointestinal tract (gut) health in the young pig. Anim Nutr. 2018;4(2):187–196. https://doi.org/10.1016/j.aninu.2017.12.004
- Kogut MH, Arsenault RJ. Gut health: the new paradigm in food animal production. Front Vet Sci. 2016;3:71. https://doi.org/10.3389/fvets.2016.00071
- Celi P, Cowieson AJ, Fru-Nji F, Steinert RE, Kluenter AM, Verlhac V. Gastrointestinal functionality in animal nutrition and health: new opportunities for sustainable animal production. Anim Feed Sci Technol. 2017;234:88–100. https://doi.org/10.1016/j.anifeedsci.2017.09.012
- Suzuki T. Regulation of the intestinal barrier by nutrients: the role of tight junctions. Anim Sci J. 2020;91(1). https://doi.org/10.1111/asj.13357
- Di Vincenzo F, Del Gaudio A, Petito V, Lopetuso LR, Scaldaferri F. Gut microbiota, intestinal permeability, and systemic inflammation: a narrative review. Intern Emerg Med. 2024;19(2):275–293. https://doi.org/10.1007/s11739-023-03374-w
- Haroun E, Kumar PA, Saba L, Kassab J, Ghimire K, Dutta D, et al. Intestinal barrier functions in hematologic and oncologic diseases. J Transl Med. 2023;21(1):233. https://doi.org/10.1186/s12967-023-04091-w
- Shi J, Barakat M, Chen D, Chen L. Bicellular tight junctions and wound healing. Int J Mol Sci. 2018;19(12):3862.
- Baxter MFA, Merino-Guzman R, Latorre JD, et al. Optimizing Fluorescein Isothiocyanate Dextran Measurement As a Biomarker in a 24-h Feed Restriction Model to Induce Gut Permeability in Broiler Chickens. Front Vet Sci. 2017;4. https://doi.org/10.3389/fvets.2017.00056
- Kuttappan VA, Vicuña EA, Latorre JD, et al. Evaluation of Gastrointestinal Leakage in Multiple Enteric Inflammation Models in Chickens. Front Vet Sci. 2015;2. https://doi.org/10.3389/fvets.2015.00066
- Wiersema ML, Kerr BJ, Koltes DA. Comparison of Intestinal Permeability Methods in Broilers over a 6-Week Growth Period. Poultry. 2023;2(3):383-394. https://doi.org/10.3390/poultry2030028
- Kuttappan VA, Berghman LR, Vicuña EA, et al. Poultry enteric inflammation model with dextran sodium sulfate mediated chemical induction and feed restriction in broilers. Poult Sci. 2015;94(6):1220-1226. https://doi.org/10.3382/ps/pev114
- Vicuña EA, Kuttappan VA, Tellez G, et al. Dose titration of FITC-D for optimal measurement of enteric inflammation in broiler chicks. Poult Sci. 2015;94(6):1353-1359. https://doi.org/10.3382/ps/pev111
- Ruff J, Barros TL, Tellez G, et al. Research Note: Evaluation of a heat stress model to induce gastrointestinal leakage in broiler chickens. Poult Sci. 2020;99(3):1687-1692. https://doi.org/10.1016/j.psj.2019.10.075
- Hernández-Ramírez JO, Nava-Ramírez MJ, Merino-Guzmán R, Téllez-Isaías G, Vázquez-Durán A, Méndez-Albores A. The effect of moderate-dose aflatoxin B1 and Salmonella Enteritidis infection on intestinal permeability in broiler chickens. Mycotoxin Res. 2019;36(1):31-39. https://doi.org/10.1007/s12550-019-00367-7
- Bhat AA, Uppada S, Achkar IW, Hashem S, Yadav SK, Shanmugakonar M, et al. Tight junction proteins and signaling pathways in cancer and inflammation: a functional crosstalk. Front Physiol. 2019;9:1942. https://doi.org/10.3389/fphys.2018.01942
- Wideman RF, Al-Rubaye A, Kwon YM, Blankenship J, Lester H, Mitchell KN, et al. Prophylactic administration of a combined prebiotic and probiotic, or therapeutic administration of enrofloxacin, to reduce the incidence of bacterial chondronecrosis with osteomyelitis in broilers. Poult Sci. 2015;94(1):25–36. https://doi.org/10.3382/ps/peu025
- Wideman RF, Hamal KR, Stark JM, Blankenship J, Lester H, Mitchell KN, et al. A wire-flooring model for inducing lameness in broilers: evaluation of probiotics as a prophylactic treatment. Poult Sci. 2012;91(4):870–883. https://doi.org/10.3382/ps.2011-01907
- Baxter MFA, Dridi S, Koltes DA, Latorre JD, Bottje WG, Greene ES, et al. Evaluation of intestinal permeability and liver bacterial translocation in two modern broilers and their jungle fowl ancestor. Front Genet. 2019;10. https://doi.org/10.3389/fgene.2019.00480
- Xi Y, Yan J, Li M, Ying S, Shi Z. Gut microbiota dysbiosis increases the risk of visceral gout in goslings through translocation of gut-derived lipopolysaccharide. Poult Sci. 2019;98(11):5361–5373. https://doi.org/10.3382/ps/pez357
Jaime Andrés Ángel Isaza
innovacion@promitec.com.co