Resumen
La inflamación es un proceso vital del sistema inmune que conlleva un importante costo metabólico en los seres vivos. La inflamación, ya sea por agentes infecciosos u otros estímulos, activa diversas células del sistema inmune, como macrófagos y neutrófilos (heterófilos en las aves), que consumen una gran cantidad de energía. Esta mayor demanda de energía se refleja en la producción de mediadores inflamatorios y en la reprogramación metabólica de las células afectadas.
A nivel sistémico, la inflamación puede causar efectos como la degradación de la proteína muscular (catabolismo), la disminución del consumo de alimento, afectar la eficiencia alimenticia y la generación de un estado de hipermetabolismo (aumento de la tasa metabólica basal), lo cual afecta negativamente a la salud y la productividad, especialmente en casos de inflamación crónica. Además, la resolución de la inflamación requiere recursos adicionales para reparar los tejidos dañados, lo que prolonga la carga metabólica.
En conclusión, es crucial controlar la inflamación excesiva mediante una inmunomodulación adecuada para minimizar los efectos secundarios y mantener la homeostasis, el rendimiento y la productividad de los animales.
Definición de inflamación
La inflamación es el conjunto de mecanismos de respuesta local y sistémica del sistema inmune (acumulación de leucocitos, proteínas plasmáticas y fluidos extracelulares derivados de la sangre y del tejido extracelular) ante una agresión infecciosa, física, química o autoinmune en los tejidos, con el objetivo de localizar, aislar y destruir un agente agresor. También tiene la función de reparar los daños causados por la activación de la inflamación (Rojas, 2023; Feehan & Gilroy, 2019). Cuando el proceso no es exitoso se da lugar a la inflamación crónica, donde el organismo continúa generando inflamación en ausencia del estímulo que la inició.

La inflamación crónica se puede definir como una respuesta inmune prolongada y persistente en la que la inflamación dura semanas, meses o incluso años. A diferencia de la inflamación aguda, que es una reacción protectora a corto plazo ante una lesión o infección, la inflamación crónica se produce cuando el desencadenante inicial no se resuelve por completo o cuando el sistema inmunitario se activa continuamente. Esta afección puede provocar daños en los tejidos, fibrosis y deterioro de la función de los órganos afectados. En los animales de producción, la inflamación crónica puede repercutir negativamente en el crecimiento, la reproducción y la salud en general, con las consiguientes pérdidas económicas para los productores.
Introducción
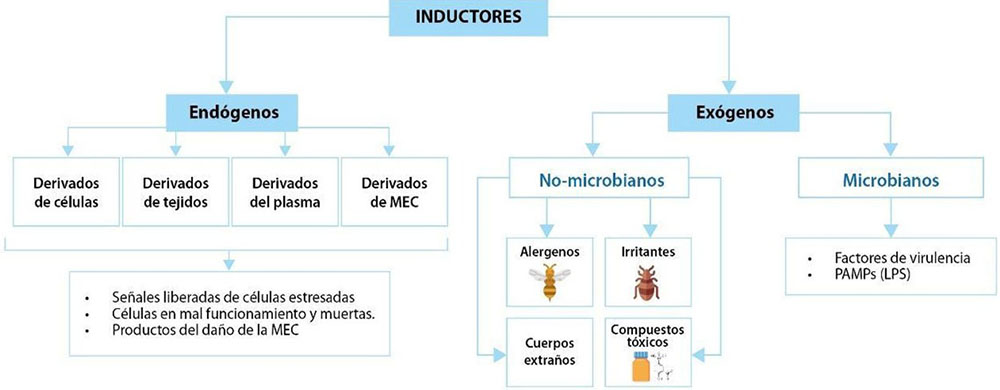
La inflamación es un proceso estratégico que ha permitido a las especies animales seguir vivas en la Tierra. La inflamación es un proceso complejo del sistema inmune que se inicia por “inductores” que pueden ser tanto exógenos: estímulos infecciosos y no infecciosos (alérgenos, toxinas, irritantes, factores antinutricionales); como endógenos: estímulos celulares, tisulares, plasmáticos o de la matriz extracelular (Figura 1). Actualmente, se conoce el funcionamiento general de la inflamación; sin embargo, aún existen lagunas en algunos conceptos y modos de acción. Si bien se entiende que el proceso inflamatorio es necesario para la vida y la homeostasis (salud), la falta de regulación podría ser bastante perjudicial para el hospedero (por ejemplo, en casos de shock séptico).

Funcionamiento básico de la inflamación
La mejor caracterización del proceso inflamatorio ha sido bajo modelos de infecciones microbianas y especialmente las de tipo bacteriano (Medzhitov, 2008). Estos microorganismos tienen estructuras comunes conocidas como patrones moleculares asociados a patógenos (PAMPs) que son detectados por receptores de reconocimiento de patrones (PRRs) expresados en células de la inmunidad innata (macrófagos y mastocitos residentes en los tejidos). Los PRR más estudiados son los receptores tipo Toll (TLR, Toll-Like Receptors) y los receptores tipo NOD (nucleotide-binding oligomerization protein domain) o NLR (NOD-like receptors). Una vez que los PRRs detectan los PAMPs, se inicia la producción de mediadores inflamatorios como quimioquinas, citoquinas, aminas vasoactivas, eicosanoides y activación del sistema de lisis celular proteolítico en cascada como el complemento (Roe, 2021).
El principal efecto de la liberación de estos mediadores es promover un exudado inflamatorio compuesto por proteínas plasmáticas y leucocitos de tipo neutrófilos en mamíferos y heterófilos en las aves, que normalmente sólo se encuentran en la sangre periférica pero que, durante el proceso inflamatorio, viajan a los tejidos donde se originó la inflamación o lesión tisular, a través de las vénulas postcapilares (Kraus y Gruber, 2021). Este proceso activa el endotelio para permitir la extravasación selectiva de neutrófilos/heterófilos e impide la salida de eritrocitos. La selectividad se produce gracias al sistema de selectinas expresadas en el endotelio e integrinas y receptores de quimioquinas expresados en los leucocitos, proceso que ocurre en la superficie del endotelio y en el espacio extravascular (donde se depositan nuevas proteínas plasmáticas que forman una matriz provisional para la unión de las integrinas expresadas por los leucocitos (Kraus y Gruber, 2021).
Una vez que llegan al tejido afectado, los neutrófilos/heterófilos se activan por contacto con el patógeno o por las citoquinas producidas por los macrófagos residentes. Los neutrófilos/heterófilos intentan eliminar el patógeno liberando compuestos que poseen almacenados internamente en gránulos, que pueden ser especies reactivas de oxígeno (ROS) y especies reactivas de nitrógeno (RNS), catepsina G y elastasas. Estos componentes son incapaces de reconocer la diferencia entre los microorganismos y los tejidos del hospedero, por lo que se produce un daño colateral inevitable a las células vecinas del hospedero (Kraus y Gruber, 2021).
El proceso culminaría exitosamente con la eliminación del estímulo inflamatorio (en este caso el microorganismo), resolución y reparación del tejido para recuperar la homeostasis, proceso que es llevado a cabo por macrófagos residentes reclutados al sitio de la inflamación (Feehan y Gilroy, 2019).
La transición de la inflamación a la resolución está mediada por mediadores lipídicos, que pasan de producir prostaglandinas (proinflamatorias) a lipoxinas (antiinflamatorias). Las lipoxinas son capaces de inhibir la llegada de nuevos neutrófilos/heterófilos, promover la llegada de nuevos monocitos de la sangre con la capacidad de eliminar células muertas (llamados barrenderos), restos celulares e iniciar la remodelación tisular. Otro grupo de moléculas conocidas como resolvinas y protectinas también ayudan al proceso de resolución de la inflamación, junto con una citoquina conocida como factor de crecimiento transformante beta (TGF-β) producida por los macrófagos (Rojas, 2017).
Si la respuesta inflamatoria es incapaz de eliminar el patógeno, el proceso toma otro curso. Los neutrófilos/heterófilos ya no llegarán al lugar, la inflamación será asumida por los macrófagos y llegarán células de la inmunidad adquirida como los linfocitos T. Si la llegada de las nuevas células es insuficiente, se producirá un proceso de inflamación crónica con formación de granulomas y órganos linfoides terciarios.
Figura 1. Representación de los inductores de la inflamación divididos en dos categorías principales: endógenos y exógenos. Inductores endógenos: Derivados de las células: señales liberadas por células estresadas, que funcionan mal o están muertas. Derivados tisulares, plasmáticos y del daño de la MEC. Inductores exógenos: No microbianos: incluyen alérgenos, irritantes, cuerpos extraños y compuestos tóxicos. Microbianos: factores de virulencia y PAMPs (como el lipopolisacárido o LPS). Los inductores desencadenan respuestas según su naturaleza, afectando a la salud del organismo. MEC: matriz extracelular, PAMP: patrones moleculares asociados a patógenos, LPS: lipopolisacárido. Adaptada de (Medzhitov, 2008).
El costo metabólico de la inflamación
El metabolismo se puede definir en simples palabras como aquellos mecanismos por los cuales el hospedero transforma nutrientes en energía. El costo metabólico podría definirse como lo que cuesta, en términos de energía y aminoácidos, llevar a cabo los procesos inflamatorios en el organismo tales como la re-epitelización, el recambio de enterocitos, el aumento de la tasa metabólica basal y el consumo de oxígeno, entre otros (Klasing, 1998).
Cuando se produce una inflamación, es un método de autoprotección del organismo para preservar la vida y restablecer la homeostasis, cuyo objetivo es eliminar estímulos nocivos como células dañadas, agentes irritantes o patógenos, e iniciar el proceso de curación. Sin embargo, esto tiene un costo energético considerable. Los siguientes puntos se consideran los más importantes:
Aumento de la demanda energética
Durante la inflamación, varias células del sistema inmune, como macrófagos, neutrófilos (heterófilos en aves) y linfocitos, se activan y proliferan. Estas células consumen cantidades significativas de energía mientras se movilizan y llevan a cabo funciones como la fagocitosis, la producción de citoquinas y la migración al lugar de la inflamación (Rojas, 2023; Leshchinsky y Klasing, 2001).
La síntesis de mediadores inflamatorios como las citoquinas, las quimioquinas y las proteínas de fase aguda requiere energía adicional. Estas moléculas desempeñan un papel clave en la coordinación y perpetuación de la respuesta inmune, pero su producción es energéticamente costosa (Klasing, 2007).
Las células inflamatorias cambian su metabolismo de un estado de reposo a un estado altamente activo. Por ejemplo, suelen pasar de la fosforilación oxidativa, que es más eficiente energéticamente, a la glucólisis, que es menos eficiente energéticamente pero más rápida. Este cambio metabólico garantiza una inmediata disponibilidad de energía para apoyar la rápida respuesta necesaria en la inflamación. Se redirigen recursos de procesos menos críticos para apoyar la respuesta inmune. Esto puede implicar que el hígado aumente la producción de proteínas de fase aguda, lo que puede reducir su capacidad para otras funciones metabólicas, como la desintoxicación hepática y el metabolismo (Klasing, 2007).
Efectos sistémicos
En casos de inflamación grave o crónica, como infecciones, sepsis, enfermedades autoinmunes o traumatismos extensos, el organismo puede entrar en un estado de hipermetabolismo. Este estado se caracteriza por un aumento de la temperatura corporal, la frecuencia cardiaca y el gasto energético. La inflamación suele provocar cambios en la utilización y el almacenamiento de nutrientes. Por ejemplo, puede aumentar la degradación de las proteínas musculares para proporcionar aminoácidos para la función inmunológica y la síntesis de proteínas de fase aguda, lo que afecta a la masa muscular y la fuerza en general (Rojas, 2017).
Costos a largo plazo
Durante la inflamación crónica, en especial en animales de larga vida como reproductores y gallinas ponedoras, puede conducir a un estado persistente de metabolismo alterado, que puede sobrecargar los recursos del organismo a largo plazo y contribuir al desarrollo de enfermedades metabólicas tipo hígado graso.
Costos asociados a la resolución de la inflamación
El organismo necesita reparar los tejidos dañados y restablecer el funcionamiento normal, lo que también requiere energía y recursos, prolongando la carga metabólica. De esta manera, el costo metabólico de la inflamación implica un aumento del gasto energético, una reprogramación metabólica y efectos sistémicos significativos que pueden afectar a la salud general del animal y su equilibrio energético. El organismo da prioridad a la respuesta inmunitaria frente a otros procesos como la ganancia de peso, la producción de huevo o la productividad en general, lo cual es beneficioso para las respuestas agudas, pero puede ser perjudicial cuando la inflamación es crónica e incontrolada.
Estrategias de modulación para un rendimiento óptimo
El control de la inflamación intestinal en los animales de producción es crucial para mantener su salud, bienestar y rendimiento productivo. La inflamación intestinal puede reducir la eficiencia de la absorción de nutrientes, afectar al crecimiento y aumentar la vulnerabilidad a las enfermedades. A continuación, se describen las estrategias clave para controlar la inflamación intestinal en animales de producción, como el pollo de engorde y las gallinas ponedoras:
1. Uso de aditivos inmunomoduladores para la inflamación
Uso de aditivos funcionales: aditivos como probióticos, prebióticos, ácidos orgánicos y enzimas mejoran la salud intestinal y refuerzan la barrera intestinal, reduciendo la inflamación.
Ácidos grasos omega-3: la incorporación de aceites ricos en ácidos grasos omega-3 (como el aceite de pescado o el aceite de linaza) puede reducir la inflamación al disminuir la producción de mediadores inflamatorios e incrementar la vía de los eicosanoides, lo que favorece la producción de lipoxinas protectinas y resolvinas.
2. Mejora del bienestar de los animales
Reducción del estrés: una gestión adecuada del entorno, evitando el exceso de densidad, mejorando la ventilación y reduciendo los factores estresantes, son elementos clave para evitar la inflamación crónica asociada al estrés.
Bioseguridad: el mantenimiento de prácticas estrictas de bioseguridad puede prevenir infecciones intestinales, como la coccidiosis o la enteritis bacteriana, que desencadenan procesos inflamatorios (Mesa-Pineda et al., 2021).
3. Uso de productos fitogénicos y naturales
Lignanos: algunos lignanos de la corteza de árboles específicos tienen propiedades antiinflamatorias y antioxidantes, lo que los convierte en herramientas útiles para reducir la inflamación intestinal. Estos compuestos de origen vegetal, con propiedades antioxidantes y antiinflamatorias, ayudan a modular la respuesta inmunitaria y contribuyen a reducir el daño celular causado por los procesos inflamatorios mediante la inhibición del factor de transcripción NFkB y el incremento de Nrf2, un factor de transcripción que incrementa la capacidad antioxidante del hospedero.
Extractos vegetales: los productos derivados de plantas, como los aceites esenciales de orégano, tomillo, ajo y cúrcuma, pueden reducir la inflamación intestinal modulando la microbiota y mejorando la inmunidad.
4. Modulación de la microbiota intestinal
Probióticos y prebióticos: los probióticos (bacterias beneficiosas) y los prebióticos (sustratos que favorecen el crecimiento de estas bacterias) ayudan a mantener una microbiota equilibrada y reducen la incidencia de la inflamación al limitar el crecimiento de patógenos.
Simbióticos: La combinación de probióticos y prebióticos puede ser más eficaz para proteger la mucosa intestinal y prevenir las respuestas inflamatorias.
5. Control de las infecciones intestinales
Vacunación y control de patógenos: mantener bajo control las infecciones gastrointestinales mediante programas de vacunación y tratamientos profilácticos reduce los focos de inflamación intestinal.
Antibióticos específicos: en casos graves de inflamación causada por infecciones bacterianas, los antibióticos de espectro estrecho pueden utilizarse con moderación para tratar las infecciones sin afectar negativamente a la microbiota intestinal.
6. Control y manejo del agua
Calidad del agua: el agua limpia y libre de contaminantes es esencial para prevenir la irritación e inflamación intestinal. Es importante tratar y mantener los sistemas de suministro de agua en condiciones óptimas.
El control de la inflamación intestinal en los animales de producción requiere un enfoque holístico que combine mejoras en la nutrición, la gestión medioambiental, el control de infecciones y el uso de aditivos funcionales inmunomoduladores. La aplicación de estrategias naturales y sostenibles, como el uso de lignanos y aceites esenciales, es una tendencia creciente que ayuda a mejorar la salud digestiva y a reducir la dependencia de los antibióticos en la producción animal.
Conclusión
La inflamación es un proceso complejo con varias etapas que pueden salirse de control. El resultado final es un equilibrio entre el hospedero y el estímulo inflamatorio. El resultado obtenido durante la inflamación vendrá determinado por la capacidad del sistema inmune y la inmunomodulación realizada para evitar en lo posible los efectos colaterales, lo que permitirá recuperar la salud y la homeostasis y, por tanto, la productividad.
Referencias
- 1. Rojas, W. (2023). Capítulo 9: Inflamación. En J. M. Anaya, L. M. Gómez Osorio, B. H. Aristizábal, L. E. Cano, D. E. Lopera (Ed.), Inmunología de Rojas (19 edición, pp. 113-128). CIB Fondo Editorial.
- 2. Feehan, K. T., & Gilroy, D. W. (2019). Is resolution the end of inflammation?. Trends in molecular medicine, 25(3), 198-214.
- 3. Medzhitov, R. (2008). Origin and physiological roles of inflammation. Nature, 454(7203), 428-435. doi: 10.1038/nature07201
- 4. Roe, K. (2021). An inflammation classification system using cytokine parameters. Scandinavian journal of immunology, 93(2). doi: 10.1111/sji.12970
- 5. Kraus, R. F., & Gruber, M. A. (2021). Neutrophils—from bone marrow to first-line defense of the innate immune system. Frontiers in immunology, 12, 767175. doi: 10.3389/fimmu.2021.767175
- 6. Rojas, W. (2017). Capítulo 15: Nutrición respuesta inmune. En L. M. Gómez Osorio. Inmunología de Rojas (18 edición). CIB Fondo Editorial.
- 7. Klasing, K. C. (1998). Nutritional modulation of resistance to infectious diseases. Poultry science, 77(8), 1119-1125. doi: 10.1093/ps/77.8.1119
- 8. Leshchinsky, T. V., & Klasing, K. C. (2001). Divergence of the inflammatory response in two types of chickens. Developmental & Comparative Immunology, 25(7), 629-638. doi: 10.1016/S0145-305X(01)00023-4
- 9. Klasing, K. C. (2007). Nutrition and the immune system. British poultry science, 48(5), 525-537. doi: 10.1080/00071660701671336
- 10. Mesa-Pineda, C., Navarro-Ruíz, J. L., López-Osorio, S., Chaparro-Gutiérrez, J. J., & Gómez-Osorio, L. M. (2021). Chicken coccidiosis: from the parasite lifecycle to control of the disease. Frontiers in Veterinary Science, 8. doi: 10.3389/fvets.2021.787653