Introducción
La industria avícola moderna está continuamente amenazada por una serie de enfermedades infecciosas. La enteritis necrótica (EN) es una de las enfermedades entéricas más importantes en la producción avícola que afecta tanto al rendimiento de la producción como al bienestar animal. Se estima que su costo global supera los US $6 mil millones cada año, lo que equivale a una pérdida de US $0.0625 por ave (Wade & Keyburn, 2015). Los brotes de EN de los que se han reportado en la literatura científica tratan sobre los sistemas de producción de pollos de engorde, pero la enfermedad también se ha observado con frecuencia en pavos (Gazdzinski y Julian, 1992), codornices (Berkhoff, 1985) (Shivaprasad et al., 2008), pollitas ponedoras comerciales (Abdul-Aziz y Barnes, 2018), gallinas ponedoras y aves silvestres (Wobeser y Rainnie, 1987) (Work et al., 1998) (Asaoka et al., 2004).
Agente etiológico
El Clostridium perfringens es el agente causante de muchas enfermedades histotóxicas y enterotóxicas en animales de producción, así como en humanos (Songer, 1996). Es una bacteria grampositiva, anaeróbica y formadora de esporas. Debido a su alta resiliencia, las esporas bacterianas son omnipresentes en el medio ambiente y a menudo se pueden encontrar en muestras de suelo y agua (Matches et al., 1974) (Voidarou et al., 2011). Además, el C. perfringens forma parte de la microbiota intestinal normal de los vertebrados, alcanzando números de hasta 105 ufc/g en el contenido intestinal de pollos sanos (Si et al., 2007). Dentro de esta especie se han caracterizado diferentes toxinotipos en función de su perfil de producción de toxinas (Rood et al., 2018).
La enteritis necrótica aviar es causada tanto por C. perfingens tipo A como por el tipo G, produciendo respectivamente toxina alfa o toxina alfa y toxina NetB. Recientemente, se propuso una distinción entre la EN inducida por el toxinotipo basado en diferencias sutiles en la descripción de la enfermedad y los informes histopatológicos en toda la literatura (Goossens et al., 2019).
La enfermedad
Se pueden distinguir dos formas de EN en función de la gravedad de la enfermedad: la forma clínica y la subclínica. La EN clínica es una enfermedad peraguda, en la que las aves caen muertas dentro de una a dos horas después de mostrar signos de malestar. Las aves muestran repentinamente una disminución en el estado de bienestar general, caracterizada por un aumento del amontonamiento, depresión, incoordinación, disminución del apetito, anorexia, deshidratación, plumas erizadas y diarrea (Long, 1973) (Porter, 1998).
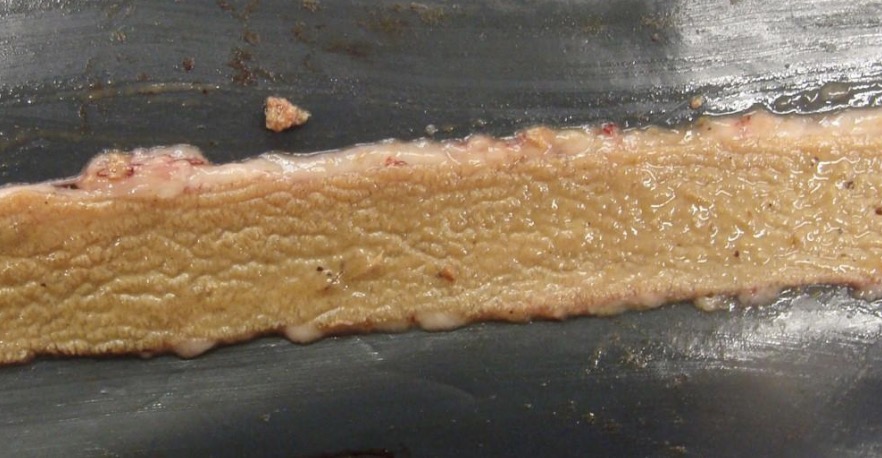
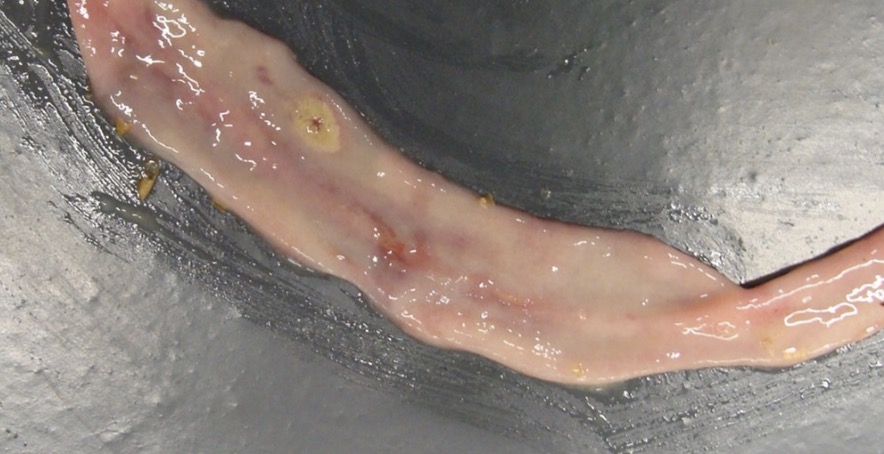
El examen post mortem de los cadáveres revela intestinos de paredes delgadas y abombamiento de los ciegos debido a una mayor producción de gas (Wijewanta & Seneviratna, 1971). Las lesiones y úlceras necróticas cubren el revestimiento del intestino delgado (duodeno, yeyuno e íleon), lo que conduce a la formación de grandes parches de tejido necrótico (Figura 1a) (Long et al., 1974). No se pueden ver signos premonitorios antes del desarrollo de la EN, aunque algunos argumentan que la cama húmeda puede ser un signo no específico de infección (Timbermont et al., 2011).
Las aves que padecen la forma subclínica de EN no muestran ningún signo de malestar ni tasas de mortalidad elevadas. Sin embargo, estas aves también sufren lesiones necróticas (Figura 1b), intestinos de paredes delgadas y daño crónico de la mucosa en el intestino delgado. La EN subclínica conducirá a una ingesta reducida de alimentos y una mala absorción de nutrientes, lo que dará como resultado una mayor tasa de conversión de alimentos (~10 %) y una caída en el aumento de peso corporal (~12 %) (Skinner et al., 2010) (Dierick et al., 2019). Aunque en su mayoría no se detecta debido a su falta de manifestación clínica, la EN subclínica actualmente tiene una importancia económica considerable para la industria avícola. Las parvadas infectadas tendrán mayores costos de alimentación, un menor rendimiento de producción de carne y, a veces, costos relacionados con el uso de productos terapéuticos para combatir la enfermedad. Además, la EN subclínica se ha asociado con poca frecuencia con la colangiohepatitis (Timbermont et al., 2011). Las bacterias pueden llegar al conducto biliar y al torrente sanguíneo portal, infectando tanto la vesícula biliar como el hígado. El hígado se vuelve pálido, agrandado y contiene un patrón reticular de focos blancos y rojos (Lövland & Kaldhusdal, 1999). Simultáneamente, se ha observado necrosis fibrinoide, infiltración de heterófilos y linfocitos, hiperplasia del conducto biliar y fibrosis con proliferación de fibra de reticulina (Onderka et al., 1990). Solo en el sacrificio, se percibe este estado, lo que lleva a una mayor tasa de decomisos.
Patogénesis en pollos de engorde
Aunque se ha investigado ampliamente, aún no se comprende completamente la patogénesis de la EN derivada de C. perfringens tipo G en pollos de engorde. C. perfringens es un miembro de la microbiota intestinal normal que alcanza números de hasta 105 ufc/g de contenido intestinal en pollos sanos (Shane et al., 1984) (Si et al., 2007). Se puede recuperar una amplia gama de genotipos de C. perfringens del contenido intestinal de aves sanas, lo que indica una gran diversidad dentro de esta población bacteriana (Nauerby et al., 2003). Todas las cepas producen toxina alfa, pero solo una pequeña fracción de esta población es capaz de producir la toxina NetB esencial y sus factores de virulencia asociados (Keyburn et al., 2010).
El contenido intestinal de los animales enfermos puede contener hasta 109 ufc de C. perfringens por gramo (Si et al., 2007). La dominancia de una sola cepa se observa en parvadas contaminadas, un proceso en el que solo una cepa virulenta supera a todas las demás cepas (Nauerby et al., 2003). La inhibición de las cepas estrechamente relacionadas puede ser facilitada por las bacteriocinas, que son toxinas proteináceas producidas por bacterias. Se ha demostrado la capacidad de las cepas virulentas de C. perfringens para secretar tales factores inhibidores del crecimiento (Barbara et al., 2008) (Timbermont et al., 2009) (Timbermont et al., 2014).
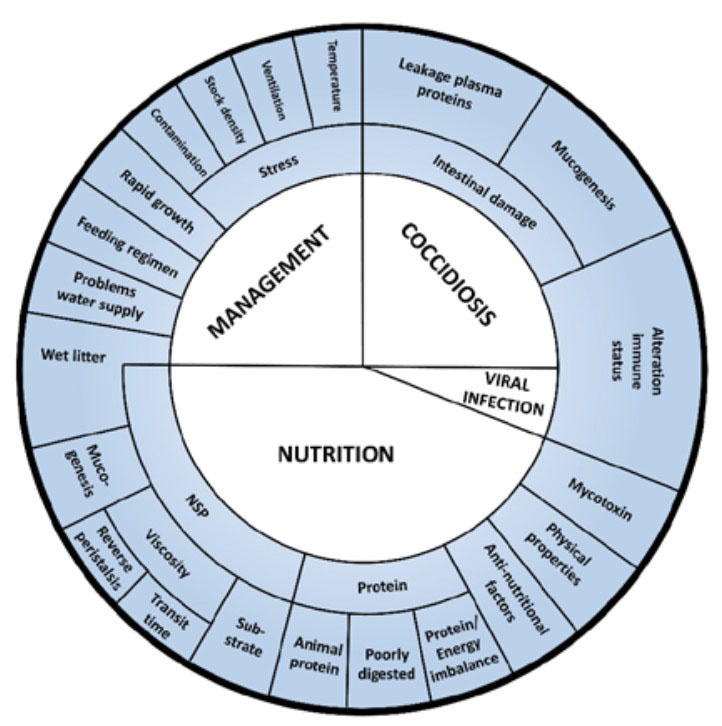
La EN es una enfermedad multifactorial, que requiere tanto la presencia de la cepa virulenta C. perfringens en el tracto gastrointestinal como un entorno favorable en el que la cepa virulenta pueda prosperar. Este entorno puede ser creado por una serie de factores predisponentes. Aquí, la infección por Eimeria se toma como ejemplo de cómo se puede alterar el ambiente intestinal a favor de la bacteria. Se sabe que el ciclo de vida intracelular de los parásitos Eimeria induce daño a las células epiteliales intestinales y, por lo tanto, aumenta la permeabilidad del revestimiento intestinal. En consecuencia, las proteínas plasmáticas se filtran en el lumen del intestino del pollo. También se activan las células caliciformes, lo que conduce a un aumento de la mucogénesis (Collier et al., 2008). Ambos procesos mejoran la cantidad de nutrientes disponibles en el tracto gastrointestinal que la bacteria puede utilizar. C. perfringens es auxotrófico, careciendo de la capacidad de producir 13 de 20 aminoácidos esenciales (Shimizu et al., 2002).
Sin embargo, C. perfringens es capaz de utilizar estos nutrientes recién disponibles mediante la producción de una serie de enzimas que incluyen varias proteasas (Collier et al., 2008). Además, los genes en los loci de patogenicidad codificados por plásmidos codifican mucinasas y múltiples glicosil hidrolasas como sialidasas y proteínas similares a quitinasa, que pueden desempeñar un papel en la degradación de la mucina (Lepp et al., 2010) (Prescott et al., 2016). Se necesita investigación adicional para verificar la función exacta de estas enzimas. No obstante, su importancia clave durante las primeras etapas de la patogénesis es probable. La disponibilidad repentina de sustrato es esencial para la proliferación masiva de C. perfringens, lo que resulta en una perturbación abierta del equilibrio microbiano. Tanto el daño predisponente como la degradación de la capa protectora de moco por la bacteria pueden exponer numerosos sitios de unión tanto para C. perfringens como para sus toxinas y factores de virulencia. C. perfringens es capaz de unirse tanto a las células epiteliales intestinales como a las moléculas de la matriz extracelular expuestas, lo que resulta en la colonización de la superficie de la mucosa (Martin & Smyth, 2010).

La proliferación masiva podría provocar el agotamiento de nutrientes. Para evitar este problema, la bacteria favorecerá la virulencia sobre el crecimiento cuando se alcance el tamaño crítico de la población. La expresión génica puede regularse mediante la detección de quórum, un proceso en el que las bacterias cercanas producen y perciben moléculas autoinductoras, lo que indica su presencia. En el pasado, la toxina alfa se consideraba el principal factor de virulencia involucrado en la patogénesis de C. perfringens. Sin embargo, en los pollos de engorde, los mutantes de la toxina alfa aún son capaces de inducir la EN, lo que cuestiona su importancia (Keyburn et al., 2006). Se ha descrito que la toxina β (netB) de C. perfringens en la enteritis necrótica, una toxina formadora de poros, es esencial para la inducción de EN (Keyburn et al., 2008) (Keyburn et al., 2010). La función exacta durante la patogénesis y los posibles socios de unión de NetB aún no están claros. Sin embargo, se ha sugerido que lo más probable es que NetB no se dirija a las células epiteliales intestinales (Prescott et al., 2016). Además de los genes de la toxina, las cepas virulentas netB+ C. perfringens codifican una serie de genes asociados a la virulencia (Lepp et al., 2010). Se necesita más investigación para revelar sus diferentes funciones.

La infiltración de toxinas y otros factores de virulencia conducirá además a la migración de C. perfringens a través del tejido. La literatura que describe las lesiones microscópicas de las últimas etapas de la patología de la EN fue combinada para establecer un modelo de patogénesis general (Figura 2) (Shane et al., 1985) (Cooper & Songer, 2009) (Timbermont et al., 2011) (M ‘Sadeq et al., 2015) (Prescott et al., 2016). Con base en los exámenes histopatológicos, se sugiere que el daño a las vellosidades se inicia en la membrana basal y en el lado lateral de los enterocitos, lo que lleva a una mayor propagación a lo largo de la lámina propia (Olkowski et al., 2008). Además, se observa transmigración de granulocitos. Tanto los enterocitos como las moléculas de la matriz extracelular son destruidas y las células inflamatorias quedan atrapadas en una red de fibrina.
Curiosamente, se ha sugerido que la destrucción de la matriz en sí misma sería responsable de la degeneración de los enterocitos en lugar de los efectos de las toxinas. Las puntas de las vellosidades se vuelven necróticas a causa de una mayor destrucción de la lámina propia. Se puede distinguir una línea de demarcación clara de células inmunitarias heterofílicas, que divide el tejido sano del necrótico. Los vasos sanguíneos se están congestionando tanto en la lámina propia como en la submucosa. Aunque C. perfringens se acumula en las zonas necróticas, no invade las células sanas. Eventualmente, la capa superficial de la mucosa se vuelve necrótica y se desprende. La degeneración celular puede alcanzar la mucosa muscular y la submucosa en una etapa posterior.
Factores predisponentes
La EN es una enfermedad multifactorial en la que la presencia de la cepa virulenta C. perfringens es insuficiente para inducir la enfermedad. Se han descrito muchos factores predisponentes capaces de modificar el entorno gastrointestinal, que se pueden dividir en factores infecciosos, factores ambientales y factores nutricionales.
Factores infecciosos
En primer lugar, los brotes de EN a menudo se asocian con la ocurrencia de coccidiosis (Al-Sheikhly & Al-Saieg, 1980). El parásito Eimeria tiene un ciclo de reproducción intracelular, lo que resulta en daño a las células epiteliales y cambios en el estado inmune del animal. Las proteínas plasmáticas se filtrarán en el lumen. Además, se estimulará la mucogénesis. Ambos procesos causan un alto aporte de nutrientes, lo que resulta en la proliferación de la cepa virulenta C. perfringens (Collier, Hofacre, Payne, Anderson y Kaiser, 2008). La inmunosupresión inducida por infecciones virales como la enfermedad infecciosa de la bursa, la enfermedad de Marek, la anemia infecciosa del pollo y la enfermedad de Gumboro también se han asociado con el desarrollo de la enfermedad EN (M ‘Sadeq, Wu, Swick y Choct, 2015).
Factores ambientales
Las características relacionadas con el manejo, como el mal control de la temperatura y la ventilación, los problemas con el suministro de agua y la naturaleza de los regímenes de alimentación, pueden estar relacionadas con los brotes de la EN. (Tsiouris et al., 2014) (Tsiouris, 2016). La cría de los animales en condiciones subóptimas puede inducir estrés a los polluelos jóvenes, lo que resulta en un período de elevada susceptibilidad de EN. Incluso la transición entre el pienso inicial y el pienso de levante puede inducir un período muy estresante. También se ha demostrado que una alta densidad de población y una rápida tasa de crecimiento predisponen a los pollos de engorde a padecer de EN (Tsiouris et., 2015) (Dierick et al., 2019).

Factores dietéticos
Una amplia variedad de factores nutricionales se correlaciona con el desarrollo de la EN (McDevitt et al., 2006). Los niveles excesivos de proteína que llegan a las partes inferiores del tracto gastrointestinal pueden conducir a la proliferación de C. perfringens. Las proteínas de origen animal, como la harina de pescado, parecen ser desencadenantes particularmente fuertes para la EN (Drew et al., 2004). Además, las proteínas mal digeridas pueden terminar en la parte distal del intestino, convirtiéndose en una fuente de proteínas para las bacterias patógenas después de la degradación en amoníaco y en aminas (Williams et al., 2001) (Juskiewicz & Jankowsk, 2004). Faltan estudios sobre los efectos de los ingredientes de proteínas vegetales, como la proteína de soya, sobre la incidencia de enteritis necrótica in vivo. Probablemente, la distribución de aminoácidos de las fuentes de proteínas es importante, ya que la naturaleza auxotrófica de C. perfringens para más de 10 aminoácidos causa una dependencia de la bacteria para aminoácidos específicos. Además, la mala digestión y absorción de proteínas del intestino delgado por parte de las enzimas del huésped puede ser predisponente, ya que entonces estarán disponibles para el crecimiento bacteriano. Evidentemente, cuanto mayor sea la concentración de proteínas en la dieta, mayor será el riesgo de desarrollo de enfermedades. Por lo tanto, una relación desequilibrada de energía a proteína del pienso, puede resultar en niveles más altos de proteína intestinal debido a una mayor ingesta de alimento por parte del ave para cumplir con sus requisitos energéticos (McDevitt et al., 2006).
El desarrollo de la EN es más común en pollos de engorde alimentados con dietas que contienen altas cantidades de polisacáridos no amiláceos (NSP) como cebada, trigo, centeno y avena (Riddell & Konga, 1992). El huésped no puede hidrolizar los NSP. Sin embargo, se ha sugerido que los NSP pueden actuar como sustrato para la microbiota patógena (Howard et al., 1995). El alimento que contiene altas cantidades de NSP tendrá un nivel de viscosidad más alto (Sasaki & Kohyama, 2012). La difusión reducida de enzimas y nutrientes puede causar una disminución en la absorción de nutrientes por parte del huésped, dejando eventualmente nutrientes para que prolifere el C. perfringens (Kumar et al., 2012). El aumento de la viscosidad del alimento también puede inducir una peristalsis inversa, trasladando las comunidades microbianas de los sitios distales a los más proximales del intestino y prolongando el tiempo de tránsito, mejorando el tiempo de interacción entre la microbiota y el sustrato (Broom, 2017). Debido a sus propiedades hidrofílicas, se sugiere que el NSP puede aumentar el contenido de agua del alimento (McDevitt et al., 2006). Esto induce una mayor ingesta de agua por parte de las aves, lo que conduce a una cama húmeda, el ambiente ideal para la esporulación del C. perfringens (Moore, 2016).
Cuando se administró pienso inoculado con C. perfringens a pollos de engorde durante 3 días consecutivos, la mortalidad varió de 0 a 12.5 % en pollos de engorde alimentados con una dieta basada en maíz, mientras que la mortalidad en animales alimentados con una dieta con altas cantidades de trigo, centeno o cebada varió de 26 a 35 % (Riddell y Konga, 1992). En un estudio similar, la mortalidad en pollos de engorde alimentados con una dieta basada en maíz fue del 2,9%, mientras que reemplazar la mitad del maíz por trigo resultó en una mortalidad del 18,1% (Branton et al., 1987).
En un estudio epidemiológico en Noruega, se demostró que la proporción de trigo y cebada con respecto al maíz se correlacionó positivamente con la incidencia de enteritis necrótica (Kaldhusdal y Skjerve, 1996). Las enzimas, como la xilanasa, se pueden utilizar para descomponer el NSP. La adición de enzimas a las dietas basadas en granos que no son de maíz puede reducir la viscosidad de la digesta y aumentar la velocidad de paso de la digesta, al tiempo que reduce significativamente la población bacteriana en el intestino delgado (Bedford y Classen, 1992; Choct et al., 1999). La suplementación de xilanasa a la alimentación de aves de corral redujo la fermentación en el intestino delgado pero aumentó la fermentación cecal (Choct et al., 1999). Se ha demostrado que esto reduce el número de C. perfringens en el intestino delgado, pero no siempre confiere protección contra la enteritis necrótica (Riddell y Konga, 1992; Jackson et al., 2003).
Otra posible explicación de los diferentes efectos de los tipos de cereales sobre la enteritis necrótica asociada a C. perfringens se debe a la posible existencia de sustancias anti-Clostridium en el maíz digerido, o sustancias proliferativas en el trigo o la cebada digerida. De hecho, la proliferación de C. perfringens en el maíz digerido fue significativamente menor que la proliferación en el trigo o la cebada digeridos (Annett et al., 2002).
Otros compuestos dietéticos que han demostrado predisponer a los pollos de engorde a la EN son las lectinas, los taninos, los inhibidores de la proteasa, los glucosinolatos, los alcaloides, los terpenos y los polifenoles (M ‘Sadeq et al., 2015). Además, los metabolitos fúngicos secundarios, las micotoxinas, también pueden iniciar la predisposición al daño intestinal (Antonissen et al., 2014). Adicionalmente, las características físicas de la dieta, como el tamaño de partícula, pueden influir en la sensibilidad a la EN (McDevitt et al., 2006). Los piensos finamente molidos (molino de martillos) aumentaron la mortalidad asociada con la enteritis necrótica en comparación con los piensos molidos gruesos (molino de rodillos) (Branton et al., 1987). Engberg et al. (2002) no encontraron efectos en la molida del pienso en los recuentos de C. perfringens en el intestino, pero encontraron una mayor digestibilidad y una disminución del número de bacterias C. perfringens en el intestino cuando las aves fueron alimentadas con pellets en lugar de gránulos.
Además, los aditivos dietéticos son una parte importante de la dieta que puede afectar la cantidad de C. perfringens y la enfermedad.
Cuando hay evidencia de desarrollo de EN, toda la parvada puede tratarse con antimicrobianos terapéuticos. Se han evaluado una variedad de antimicrobianos en modelos de la enfermedad y se utilizan en el campo en caso de un brote de la enfermedad (Cooper & Songer, 2009) (Paiva & McElroy, 2014). Como las medidas preventivas son claramente mucho más importantes, en este documento no nos centraremos en el tratamiento.
Los promotores de crecimiento antimicrobianos se han utilizado profilácticamente en toda la industria avícola durante décadas. Debido a la creciente preocupación por la resistencia a los antibióticos, su uso está prohibido en la Unión Europea y en muchas otras partes del mundo (Casewell et al., 2003). Por lo tanto, hay una gran demanda de medidas alternativas para hacer frente a las infecciones por C. perfringens.
En primer lugar, la optimización de las prácticas de manejo, y específicamente la bioseguridad y el saneamiento en la granja, puede reducir la exposición a posibles factores de riesgo (Eimeria, virus y las propias bacterias causantes). El aumento de las medidas higiénicas puede limitar la propagación de patógenos virulentos y, posteriormente, reducir la exposición de los animales (McDevitt et al., 2006). Se debe evitar el reciclaje de la cama. (Cooper & Songer, 2009).
En segundo lugar, limitar los efectos de los factores predisponentes también puede ser una buena estrategia para reducir la incidencia de EN. El efecto predisponente del estrés debido a factores relacionados con la gestión se puede reducir fácilmente manteniendo buenas prácticas de cría. La implementación de un programa de control de la coccidiosis puede reducir el daño intestinal inicial de la mucosa, un paso clave en la patogénesis EN. Se ha demostrado que las cepas de C. perfringens son sensibles a los fármacos anticoccidiales ionóforos (Martel et al., 2004). La restricción de su uso aumentará la susceptibilidad de las parvadas de pollos de engorde a la EN (McDevitt et al., 2006). La asociación entre ambas enfermedades debe tenerse en cuenta al implementar programas de vacunación teniendo en cuenta el posible daño a la mucosa por cepas de vacunas atenuadas (Van Immerseel et al., 2004).
Además, el efecto predisponente de los factores nutricionales se puede reducir optimizando las formulaciones de la dieta, excluyendo los ingredientes de riesgo y controlando los niveles de micotoxinas. Se ha demostrado que la adición de enzimas al alimento reduce las proteínas y los carbohidratos no digeribles en la parte distal de los tractos gastrointestinales, lo que finalmente reduce el riesgo de brotes de EN. Ejemplos de tales enzimas alimentarias son xilanasas, β-mananasas y proteasas (Sinlae & Choct, 2000) (Jackson et al., 2003).
Otro enfoque para prevenir la proliferación de C. perfringens es alterar la composición de la microbiota intestinal (Caly et al., 2015). Algunos probióticos, suplementos alimentarios microbianos que mejoran este equilibrio microbiano, están disponibles comercialmente y tienen actividad documentada en modelos de enfermedades (Layton et al., 2013) (Tactacan et al., 2013) (Caly et al., 2015) (Wang et al., 2017). Los prebióticos son “ingredientes alimenticios indigeribles que estimulan selectivamente el crecimiento y la actividad de las bacterias beneficiosas que residen en el intestino” (Gibson & Roberfroid, 1995). Hasta la fecha, no hay prebióticos disponibles comercialmente contra la EN, aunque la suplementación dietética de manano-oligosacáridos (MOS) ha demostrado ser parcialmente efectiva (Kim et al., 2011). Posteriormente, se ha investigado ampliamente la administración oral de productos de exclusión competitiva, una suspensión de la microbiota intestinal de animales sanos (Hofacre et al., 1998) (Kaldhusdal et al., 2001) (McReynolds et al., 2009).
Por último, el desarrollo de una estrategia basada en la vacunación contra la EN está en fase de investigación. La vacunación subcutánea (día 1-3-15) con toxoide alfa o NetB recombinante ha demostrado ser parcialmente protectora contra la EN inducida experimentalmente (Mot et al., 2014). A pesar de los resultados prometedores, la implementación de estrategias de vacunación en la industria avícola es un desafío teniendo en cuenta el régimen de dosis y el alto costo de mano de obra. La vacunación al día uno de la eclosión parece insuficiente para protegerse de EN (Mot et al., 2013). Es necesario realizar una investigación exhaustiva para investigar más a fondo las perspectivas de las estrategias de vacunación oral que son aplicables en el campo, es decir, la naturaleza de los vectores que se utilizarán y la combinación óptima de antígenos.
Referencias

Filip Van Immerseel
Universidad de Ghent, Departamento de Pato-biología, Farmacología y Medicina Zoológica, Equipo de Salud Intestinal Ganadera (LiGHT por sus siglas en inglés), Merelbeke, Bélgica.
Filip.vanimmerseel@ugent.be